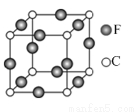
根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结 论 |
A | 取少量食盐溶于水,加稀硫酸酸化,再滴入淀粉溶液,溶液未呈蓝色 | 该食盐中不含有碘酸钾 |
B | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,下层溶液显紫红色 | Fe3+的氧化性大于I2 |
C | 向蛋白质溶液中加入CuCl2或(NH4)2SO4饱和溶液,均有沉淀 | 蛋白质均发生了变性 |
D | 将0.1 mol·L-1,MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1 mol • L-1CuSO4溶液,白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
A. A B. B C. C D. D
在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,发生如下反应: CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ,测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g) ,测得n(CH4)随时间变化数据如下表:
温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) /mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) /mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法正确的是( )
A. T2时CH4的平衡转化率为70.0%
B. 该反应的△H>0、T1<T2
C. 保持其他条件不变,T1时向平衡体系中再充入0.30molCH4和0.80molH2O(g),平 衡向正反应方向移动
D. 保持其他条件不变, T1时向平衡体系中再充入0.50 mol CH4和1.20 mol NO2,与原平衡相比,达新平衡时N2的浓度增大、体积分数减小
高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面。查阅资料得到以下有关高氯酸的信息:
名称 | 分子式 | 外观 | 沸点 |
高氯酸 | HClO4 | 无色液体 | 130℃ |
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如下:

(1)操作①的名称是____________,操作②的名称是___________。
(2)反应器Ⅰ中发生反应的化学方程式为________________________。
(3)反应器Ⅱ中发生反应的离子方程式为__________________________。
(4)若反应器Ⅱ中SO2以H2O2代替也可达到同样的目,此时发生反应的离子方程式为___________。
(5)若想得到201 kg的 HClO4纯品,至少需要NaClO3_________kg。
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸。写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)______________________________。


 (R1、R2表示烃基)
(R1、R2表示烃基) CH3CH2Br
CH3CH2Br CH3CH2OH__________________
CH3CH2OH__________________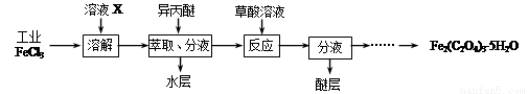

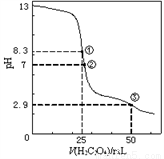
 CH3OH(g)的平衡常数K的表达式为________________;甲图是反应时CO和CH3OH(g)的物质的量浓度随时间(t)的变化曲线。从反应开始至达到平衡时,用H2表示的反应速率υ(H2)=________________。
CH3OH(g)的平衡常数K的表达式为________________;甲图是反应时CO和CH3OH(g)的物质的量浓度随时间(t)的变化曲线。从反应开始至达到平衡时,用H2表示的反应速率υ(H2)=________________。