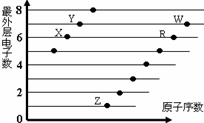
甲同学将Na2O2分别与H2O和浓盐酸反应,有如下现象:
实验序号 | 使用药品 | 现象 |
Ⅰ | Na2O2、H2O | ① |
Ⅱ | Na2O2、浓盐酸 | ①试管壁发热;②刺激性气味的气体产生;③反应后所得溶液呈浅黄绿色 |
请完成下 列问题:
列问题:
实验I中:
⑴该反应是 反应(填“放热”或“吸热”)。
⑵反应的化学方程式是: 。
⑶证明无色无味气体是氧气的方法是:  。
。
实验Ⅱ中:
⑷根据现象②、③,推测生成的气体中可能含有Cl2,产生Cl2的化学方程式是: 。
⑸若往“浅黄绿色溶液”中加入FeCl3溶液,立即产生与实验I相同的气体 ,原因是:
,原因是:  。
。
按要求完成下列空白:
⑴印刷电路板是由高分子材料和铜箔复合而成.刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2.请写出反应的离子方程式 。
⑵请写出在碱性溶液中,ClO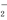 与Fe2+反应的离子方程式为: 。
与Fe2+反应的离子方程式为: 。
⑶NaAlH4是重要的还原剂。请写出NaAlH4与水发生氧化还原反应的化学方程式: 。
⑷+6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的Cr2O72-还原成Cr3+,请写出该反应的离子方程式: 。
⑸亚氯酸钠(NaClO2)溶液可作为烟气的吸收剂,并对烟气进行脱硫、脱硝。在装有亚氯酸钠溶液的鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10?3mol·L?1。反应一段时间后溶液中离子浓度的分析结果如下表。
离 | SO | SO | NO | NO | Cl? |
c/(mol·L?1) | 8.35×10?4 | 6.87×10?6 | 1.5×10?4 | 1.2×10?5 | 3.4×10?3 |
写出NaClO2溶液脱硝过程中主要反应的离子方程式 。
下列根据实验操作和现象得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 将少量Fe(NO3)2试样加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2试样已变质 |
B | 向甲苯中滴加少量酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | 甲苯发生了氧化反应 |
C | 常温下分别测定浓度均为0.1mol/L的Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3>Na2CO3 | 非金属性:Si>C |
D | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
 子
子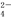


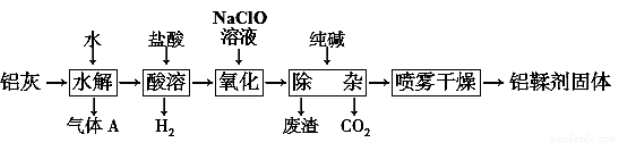
 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O
 )是临床上一种降脂抗血栓药物,它的一条合成路线如下:
)是临床上一种降脂抗血栓药物,它的一条合成路线如下: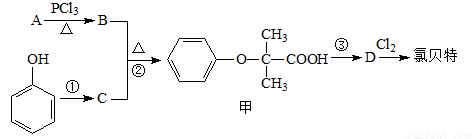

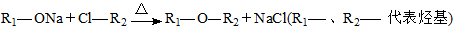
 满足以下条件的所有甲的同分异构体有 种(不考虑立体异构)。
满足以下条件的所有甲的同分异构体有 种(不考虑立体异构)。 H溶液反应的化学方程式 。
H溶液反应的化学方程式 。