将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应:
2 SO2(g)+ O2(g) 2SO3△H<0。得到如表中的两组数据:
2SO3△H<0。得到如表中的两组数据:
实验编号 | 温度/℃ | 平衡常数/mol-1·L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
下列说法不正确的是
A.x= 1.6,y=0.2 ,t<6
B.T1、T2的关系:T1 > T2
C.K1、K2的关系:K2>K1
D.实验1在前6min的反应速率υ(SO2)=0.2 mol·L-1·min-1
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
Ⅰ.配制100mL 0.10mol/L NaOH标准溶液.
Ⅱ.取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用的标准NaOH溶液进行滴定.重复上述滴定操作2~3次,记录数据如下.
实验编号 | NaOH溶液的浓度(mol/L) | NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 20.00 | |
2 | 0.10 | 22.46 | 20.00 |
3 | 0.10 | 22.54 | 20.00 |
(1)第1次实验滴定前液面在0刻度,滴定后如图所示,则第一次实验滴定完用去NaOH溶液的体积记录为_________mL。滴定达到终点的现象是_____________________。
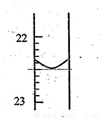
(2)根据上述数据,可计算出该盐酸的浓度为___________。
(3)在上述实验中,下列操作会造成测定结果偏高的有___________
A.滴定终点时俯视读数
B.酸式滴定管使用前,水洗后未用待测稀盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.配制NaOH标准溶液,定容时仰视
E.碱式滴定管尖嘴部分有气泡,滴定后消失
25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 mol·L-1 | K1=4.4×10-7 mol·L-1 K2=5.6×10-11 mol·L-1- | 3.0×10-8mol·L-1 |
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为________________。
(2)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母序号,下同)。
A.c(H+)
B.
C.c(H+)·c(OH-)
D.
E.
若该溶液升高温度,上述5种表达式的数据增大的是___________。
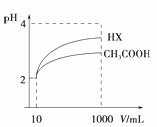
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数__________(填“大于”、“等于”或“小于”)醋酸的平衡常数。稀释后,HX溶液中由水电离出来的c(H+) __________(填“大于”、“等于”或“小于”)醋酸的溶液中由水电离出来的c(H+),理由是______________________________。
(4)已知100℃时,水的离子积为1×10-12,该温度下测得某溶液pH=7,该溶液显__________(填“酸”、“碱”或“中”)性。将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a:b=__________。
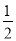 O2(g)= CO2(g)+2H2(g) △H2
O2(g)= CO2(g)+2H2(g) △H2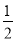 O2(g)=H2O(g) △H =-241.8 kJ·mol-1,则反应②的△H2= 。
O2(g)=H2O(g) △H =-241.8 kJ·mol-1,则反应②的△H2= 。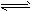 CH3OH(g),现实验室模拟该反应并进行分析,下图是该反应在不同温度下CO的转化率随时间变化的曲线
CH3OH(g),现实验室模拟该反应并进行分析,下图是该反应在不同温度下CO的转化率随时间变化的曲线