0 174647 174655 174661 174665 174671 174673 174677 174683 174685 174691 174697 174701 174703 174707 174713 174715 174721 174725 174727 174731 174733 174737 174739 174741 174742 174743 174745 174746 174747 174749 174751 174755 174757 174761 174763 174767 174773 174775 174781 174785 174787 174791 174797 174803 174805 174811 174815 174817 174823 174827 174833 174841 203614
 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
 ℃时水的电离平衡曲线应为_________(填“A”或“B”),请说明理由 。
℃时水的电离平衡曲线应为_________(填“A”或“B”),请说明理由 。 品m g,在烧杯中用蒸馏水溶解
品m g,在烧杯中用蒸馏水溶解
 H++HA-,HA-
H++HA-,HA-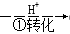 Cr2O72-
Cr2O72- Cr3+
Cr3+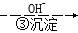 Cr(OH)3
Cr(OH)3 下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
 “电镀池”),A电极的电极反应式为 。
“电镀池”),A电极的电极反应式为 。 质属于弱电解质的是
质属于弱电解质的是 Cl2 D.FeCl2
Cl2 D.FeCl2 B.FeCl3 →FeCl2
B.FeCl3 →FeCl2 (OH)2
(OH)2