根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 将1mL乙酸乙酯分别加入6mL同浓度的NaOH溶液和稀H2SO4中,水浴加热相同时间后,碱溶液中酯层完全消失,而酸中有 | 说明酯在NaOH溶液中的水解程度大于 H2SO4溶液中 |
B | 向10mL0.2mol·L?1NaOH溶液中滴入2滴0.1 mol·L?1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol·L?1FeCl3溶液,生成红褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
C | 室温下,实验测得:0.1mol·L-1Na2CO3溶液的pH约为11.6;0.1mol·L-1 NaHCO3溶液的pH约为9.7 | CO32 |
D | 用3mL稀盐酸分别与等质量的Zn粒、Zn粉反应,Zn粉产生气体的速率快 | Zn粉的活泼性大于Zn粒 |
80℃时,NO2(g)+SO2(g) SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(NO2)/mol ·L-1 | 0.10 | 0.20 | 0.20 |
c(SO2)/mol ·L-1 | 0.10 | 0.10 | 0.20 |
A.平衡时,乙中SO2的转化率大于50%
B.当反应平衡时,丙中c(SO2)是甲中的2倍
C.温度升至90℃,上述反应平衡常数为25/16,则正反应为吸热反应
D.其他条件不变,若起始时向容器乙中充入0.10mol ·L-1 NO2和0.20 mol ·L-1 SO2,达到平衡时c(NO)与原平衡不同
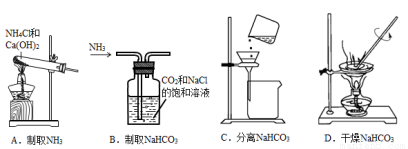
 原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下: 应的叙述相符的是( )
应的叙述相符的是( )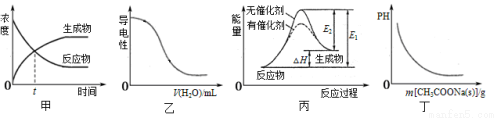

 剩余
剩余 -结合H+的能力比 HCO3-的强
-结合H+的能力比 HCO3-的强