2.实验测得:101kPa时,1mol H2完全燃烧生成液态水,放出285.8kJ的热量;1mol CH4完全燃烧生成液态水和CO2,放出890.3kJ的热量.下列热化学方程式的书写正确的是( )
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890.3kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| C. | H2(g)+12O2(g)═H2O(g)△H=-285.8kJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1 |
1.在1.0L密闭容器中放入1.0molX(g),在一定温度进行如下反应:X(g)?Y(g)+Z(g)△H=akJ.mol-1反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)实验测得,随温度的升高反应的平衡常数K增大,则△H>0(填>、<或=)
(2)其他条件不变时,为使平衡向右移动,采用的下列措施可行的是BD.
A.缩小容器容积 B.及时分离出Y、Z C.使用合理的催化剂 D.升高体系温度
(3)计算平衡时X的转化率为50%,该温度下反应的平衡常数值为:0.5.
(4)由总压强p和起始压强po表示反应体系的总物质的量n(总)和反应物X的物质的量n(X),则n(总)=$\frac{p}{{p}_{0}}$mol,n(X)=(2-$\frac{p}{{p}_{0}}$)mol,反应物X的转化率a(X)的表达式为($\frac{p}{{p}_{0}}$-1)×100%.
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 |
| 总压强p/100kPa | 4.00 | 4.20 | 4.50 | 5.20 | 6.00 | 6.00 |
(1)实验测得,随温度的升高反应的平衡常数K增大,则△H>0(填>、<或=)
(2)其他条件不变时,为使平衡向右移动,采用的下列措施可行的是BD.
A.缩小容器容积 B.及时分离出Y、Z C.使用合理的催化剂 D.升高体系温度
(3)计算平衡时X的转化率为50%,该温度下反应的平衡常数值为:0.5.
(4)由总压强p和起始压强po表示反应体系的总物质的量n(总)和反应物X的物质的量n(X),则n(总)=$\frac{p}{{p}_{0}}$mol,n(X)=(2-$\frac{p}{{p}_{0}}$)mol,反应物X的转化率a(X)的表达式为($\frac{p}{{p}_{0}}$-1)×100%.
19.如表所示是某些物质的燃烧热数据:
①煤油的组成可看作C12H26,煤油燃烧生成液态水时的热化学方程式为2C12H26(l)+37O2(g)═24CO2(g)+26H2O(l)△H=-17142.8kJ•mol-1.
②由上表中的数据能(填“能”或“不能”)计算出反应:C2H4(g)+H2(g)→C2H6(g)的反应热.若能,该反应△H=-137.0kJ•mol-1(若不能,此空不填);若不能,原因是不填(若能,此空不填).
0 173168 173176 173182 173186 173192 173194 173198 173204 173206 173212 173218 173222 173224 173228 173234 173236 173242 173246 173248 173252 173254 173258 173260 173262 173263 173264 173266 173267 173268 173270 173272 173276 173278 173282 173284 173288 173294 173296 173302 173306 173308 173312 173318 173324 173326 173332 173336 173338 173344 173348 173354 173362 203614
| 物质 | C(s) | H2(g) | C2H4(g) | C2H6(g) | C3H8(g) | C12H26(l) |
| △H/ kJ•mol-1 | -393.5 | -285.8 | -1 411.0 | -1 559.8 | -2 219.9 | -8 571.4 |
②由上表中的数据能(填“能”或“不能”)计算出反应:C2H4(g)+H2(g)→C2H6(g)的反应热.若能,该反应△H=-137.0kJ•mol-1(若不能,此空不填);若不能,原因是不填(若能,此空不填).

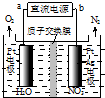 发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.
发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.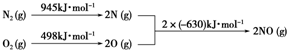

 请回答下列问题:
请回答下列问题: