10.下列实验不能获得成功的是( )
①用甲烷气体通入碘水制碘甲烷
②甲烷和溴蒸气混合光照制取纯净的一溴甲烷
③用酒精灯加热甲烷气体制取炭黑和氢气.
①用甲烷气体通入碘水制碘甲烷
②甲烷和溴蒸气混合光照制取纯净的一溴甲烷
③用酒精灯加热甲烷气体制取炭黑和氢气.
| A. | 只有① | B. | 只有③ | C. | 只有② | D. | ①②③ |
9.下列式子表示的物质一定为纯净物的是( )
| A. | C2H6 | B. | C4H10 | C. | C5H12 | D. | C7H16 |
6.SO2和NOx都是大气污染物.
(1)直接排放含SO2的烟气会形成酸雨,危害环境.用化学方程式表示SO2形成硫酸型酸雨的过程SO2+H2O?H2SO3、2H2SO3+O2=2H2SO4或2SO2+O2$\stackrel{浮尘}{?}$2SO3、SO3+H2O=H2SO4.
(2)右表是某小组同学测得的不同天气情况下的某县城空气中SO2的平均含量.请你分析雨后或风速较大时SO2平均含量较低的原因:
①雨后:可能是下雨时,二氧化硫溶于水,并与之反应降低了雨后空气中SO2的含量;
②风速较大时:风速越大,气体扩散速度越快,空气中SO2浓度越小.
(3)洗涤含SO2的烟气.以下物质不能作为洗涤剂的是cd(填字母序号).
a.熟石灰 b.纯碱c.CaCl2d.NaHSO3
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下:FeS2$→_{+O_{2}+H_{2}O}^{在微生物作用下}$Fe2++SO42-Fe2+
①该技术的第一步反应的离子方程式为2FeS2+7O2+2H2O=4H++2Fe2++4SO42-.
②处理1kg含80% FeS2的黄铁矿,第二步消耗O2(标况)的体积为37.352L(保留一位小数).
(5)某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图1所示.由图可知,光化学烟雾是指O3、醛、PAN
等污染物气体和颗粒物所形成的烟雾.

(6)氧化-还原法消除NOx的转化如下:NO$→_{反应Ⅰ}^{O_{3}}$NO2$→_{反应Ⅱ}^{CO(NH_{2})_{2}}$N2
①反应Ⅰ为NO+O3=NO2+O2,生成11.2L O2(标况)时,转移电子的物质的量是1mol.
②反应Ⅱ中,反应的化学方程式是6NO2+4CO(NH2)2=7N2+8H2O+4CO2.
(7)利用氨水可以将SO2和NO2吸收,原理如图2所示:
NO2被吸收的离子方程式是2NO2+4HSO3-=N2+4SO42-+4H+..
(1)直接排放含SO2的烟气会形成酸雨,危害环境.用化学方程式表示SO2形成硫酸型酸雨的过程SO2+H2O?H2SO3、2H2SO3+O2=2H2SO4或2SO2+O2$\stackrel{浮尘}{?}$2SO3、SO3+H2O=H2SO4.
(2)右表是某小组同学测得的不同天气情况下的某县城空气中SO2的平均含量.请你分析雨后或风速较大时SO2平均含量较低的原因:
| 天气情况 | 平均风速(m/s) | 空气中SO2的平均含量(mg/L) |
| 雨前 | ||
| 雨后 | ||
| 晴 | ||
| 晴 |
②风速较大时:风速越大,气体扩散速度越快,空气中SO2浓度越小.
(3)洗涤含SO2的烟气.以下物质不能作为洗涤剂的是cd(填字母序号).
a.熟石灰 b.纯碱c.CaCl2d.NaHSO3
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下:FeS2$→_{+O_{2}+H_{2}O}^{在微生物作用下}$Fe2++SO42-Fe2+
①该技术的第一步反应的离子方程式为2FeS2+7O2+2H2O=4H++2Fe2++4SO42-.
②处理1kg含80% FeS2的黄铁矿,第二步消耗O2(标况)的体积为37.352L(保留一位小数).
(5)某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图1所示.由图可知,光化学烟雾是指O3、醛、PAN
等污染物气体和颗粒物所形成的烟雾.

(6)氧化-还原法消除NOx的转化如下:NO$→_{反应Ⅰ}^{O_{3}}$NO2$→_{反应Ⅱ}^{CO(NH_{2})_{2}}$N2
①反应Ⅰ为NO+O3=NO2+O2,生成11.2L O2(标况)时,转移电子的物质的量是1mol.
②反应Ⅱ中,反应的化学方程式是6NO2+4CO(NH2)2=7N2+8H2O+4CO2.
(7)利用氨水可以将SO2和NO2吸收,原理如图2所示:
NO2被吸收的离子方程式是2NO2+4HSO3-=N2+4SO42-+4H+..
5.某校化学探究小组成员讨论下列Ⅰ、Ⅱ、Ⅲ、Ⅳ四种仪器装置的气体制备与性质实验的用法,其中不合理的是( )

| A. | 装置Ⅰ:可以用来验证碳的非金属性比硅强 | |
| B. | 装置Ⅱ:橡皮管的作用是使水顺利流下 | |
| C. | 装置Ⅲ:不能检查该装置的气密性 | |
| D. | 装置Ⅳ:先从①口进气收集满二氧化碳,再从②口进气,可收集NO气体 |
3.储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料.如镧镍合金,它吸收氢气可结合成金属氢化物,其化学式可近似地表示为 LaNi5H6(LaNi5H6中各元素化合价均可看作是零),它跟 NiO(OH)可组成镍氢可充电电池:
LaNi5H6+6NiO(OH)$?_{充电}^{放电}$LaNi5+6Ni(OH)2
下列说法不正确的是( )
LaNi5H6+6NiO(OH)$?_{充电}^{放电}$LaNi5+6Ni(OH)2
下列说法不正确的是( )
| A. | 反应过程中,化合价发生变化的元素是镍、镧 | |
| B. | 该电池放电时,负极反应为:LaNi5H6+6OH--6e-=LaNi5+6H2O | |
| C. | 市面上出售的标称容量为 2000 mA•h的1节镍氢电池至少应含有镧镍合金5.4 g(已知 1法拉第电量为96500库仑或安培•秒) | |
| D. | 充电电池放电后可以再充电使活性物质获得再生,但实际上充放电次数仍有限制 |
2.下列实验设计及其对应的离子方程式均正确的是( )
0 172383 172391 172397 172401 172407 172409 172413 172419 172421 172427 172433 172437 172439 172443 172449 172451 172457 172461 172463 172467 172469 172473 172475 172477 172478 172479 172481 172482 172483 172485 172487 172491 172493 172497 172499 172503 172509 172511 172517 172521 172523 172527 172533 172539 172541 172547 172551 172553 172559 172563 172569 172577 203614
| A. | 用 FeCl3溶液腐蚀铜线路板:Cu+2Fe 3+=Cu2++2Fe2+ | |
| B. | 向沸水中滴加氯化铁溶液制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3+3H+ | |
| C. | 用惰性电极电解饱和食盐水制备金属钠:2NaCl=2Na+Cl2↑ | |
| D. | 用浓盐酸酸化的 KMnO4溶液与 H2O2反应,证明 H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |



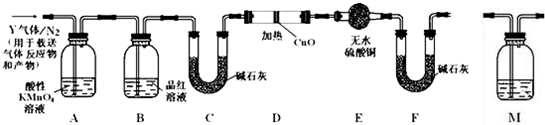
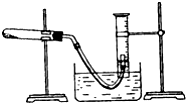 某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量.实验步骤如下:
某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量.实验步骤如下: