7.某学习小组利用如图装置进行电解氯化铵溶液的实验.其中X为铁,Y为石墨,a为wg质量分数为40%的NH4Cl(滴有酚酞).已知:①氧化性:Cl2>Br2>O2>I2,②NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2

(l)电解过程中,A 装置中可观察到的现象是X极产生无色气体,Y极产生黄绿色的气体,X极溶液变红.
(2)请选用上述仪器,组装一套检验产生氢气的装置:h→p→q→m→n→j→k→o[按气流方向(用“→”表示),用小写字母表示,装置不重复使用].
(3)某同学认为将E换成装有碱石灰的干燥管也可以达到相同效果,乙同学认为不合理,其理由是碱石灰不能除去混有的氨气,氨气与氧化铜反应产生水蒸气对实验干扰.
(4)设计实验检测阳极产生的气体成分(除水蒸气外).(所选的试剂用字母编号代替)限选试剂:
A、3mol/LNaOH溶液 B、品红 C、酸化的淀粉-KI溶液 D、KBr溶液
(5)电解结束后,加热电解液将NH3完全蒸出,并用水吸收形成200.00mL溶液,取出其中的20.00mL加指示剂后用标准浓度为c mol/L的盐酸溶液滴定,消耗盐酸V mL,则电解制得NH3的产率$\frac{107cV}{80w}$(用化简为整数的含w、c、V的代数式表示).
(6)若实验时反接了正负极,则X极的电极方程式为Fe-2e-=Fe2+.

(l)电解过程中,A 装置中可观察到的现象是X极产生无色气体,Y极产生黄绿色的气体,X极溶液变红.
(2)请选用上述仪器,组装一套检验产生氢气的装置:h→p→q→m→n→j→k→o[按气流方向(用“→”表示),用小写字母表示,装置不重复使用].
(3)某同学认为将E换成装有碱石灰的干燥管也可以达到相同效果,乙同学认为不合理,其理由是碱石灰不能除去混有的氨气,氨气与氧化铜反应产生水蒸气对实验干扰.
(4)设计实验检测阳极产生的气体成分(除水蒸气外).(所选的试剂用字母编号代替)限选试剂:
A、3mol/LNaOH溶液 B、品红 C、酸化的淀粉-KI溶液 D、KBr溶液
| 操作 | 现象和结论 |
| 将混合气体依次通入D(或B),足量的A,然后通入C | D变黄色(或B褪色),则混合气体有氯气;C变蓝,则混合气体含的氧气 |
(6)若实验时反接了正负极,则X极的电极方程式为Fe-2e-=Fe2+.
6.Na2FeO4可通过电解法制备,装置如图,下列说法正确的是( )


| A. | Pt周围的pH降低 | |
| B. | 当生成标准状况下22.4LH2时,转移的电子数为1.5 NA | |
| C. | 阳极反应式是Fe-6e-+8OH-═FeO42-+4H2O | |
| D. | 制得1mol Na2FeO4,有8molOH-从左向右通过离子交换膜 |
5.高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O═3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述正确的是( )
| A. | 放电时,正极区溶液的pH增大 | |
| B. | 放电时,负极反应式为3Zn-6e-=3Zn2+ | |
| C. | 充电时,每转移3 mol电子,阳极有1 mol Fe(OH)3被还原 | |
| D. | 充电时,电池的锌电极接电源的正极 |
3.常温下,Ksp[Mg(OH)2]=1.1×10-11,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述不正确的是( )
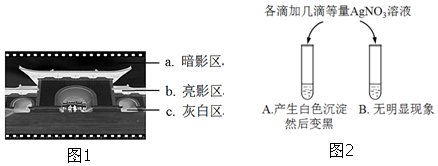
| A. | 浓度均为2×10-5mol•L-1的AgNO3溶液和NaCl溶液等体积混合,有白色沉淀产生 | |
| B. | 将0.001mol•L-1的AgNO3溶液滴入0.001mol•L-1的KCl和K2CrO4的混合溶液中,先产生AgCl沉淀 | |
| C. | c(Mg2+)为0.11mol•L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH要控制在9以上 | |
| D. | 其他条件不变,向饱和Ag2CrO4水溶液中加入少量K2CrO4溶液,溶液中c(Ag+)减小 |
2. 为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)丙烯是石化工业的主要原料之一,由于市场对丙烯的需求量激增,丙烷脱氢制丙烯的技术日益受到重视.某研究机构需得到C3H8(g)═3C(石墨,s)+4H2(g)的△H,但直接测定实验难进行,可通过图中各组物质能量总和及相互间转化中的能量变化计算得到:
①判断:△H>0(选填“>”、“<”或“=”).
②△H=△H1-△H2-△H3(用含△H1、△H2、△H3的代数式表示).
(2)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452.8KJ/mol
(3 )由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)?2NH3(g)△H=akJ•mol-1.试根据表中所列键能数据计算a的数值为:-93
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)═CO2(g)△H=-393kJ•mol-1 ①
2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1 ②
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2599kJ•mol-1 ③
根据盖斯定律,计算 298K时C(s,石墨)和H2(g)反应生成1mol C2H2(g)的焓变为+227.7kJ/mol.
 为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.(1)丙烯是石化工业的主要原料之一,由于市场对丙烯的需求量激增,丙烷脱氢制丙烯的技术日益受到重视.某研究机构需得到C3H8(g)═3C(石墨,s)+4H2(g)的△H,但直接测定实验难进行,可通过图中各组物质能量总和及相互间转化中的能量变化计算得到:
①判断:△H>0(选填“>”、“<”或“=”).
②△H=△H1-△H2-△H3(用含△H1、△H2、△H3的代数式表示).
(2)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452.8KJ/mol
(3 )由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)?2NH3(g)△H=akJ•mol-1.试根据表中所列键能数据计算a的数值为:-93
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
已知:C(s,石墨)+O2(g)═CO2(g)△H=-393kJ•mol-1 ①
2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1 ②
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2599kJ•mol-1 ③
根据盖斯定律,计算 298K时C(s,石墨)和H2(g)反应生成1mol C2H2(g)的焓变为+227.7kJ/mol.
1.下列各组离子一定能大量共存的是( )
0 163485 163493 163499 163503 163509 163511 163515 163521 163523 163529 163535 163539 163541 163545 163551 163553 163559 163563 163565 163569 163571 163575 163577 163579 163580 163581 163583 163584 163585 163587 163589 163593 163595 163599 163601 163605 163611 163613 163619 163623 163625 163629 163635 163641 163643 163649 163653 163655 163661 163665 163671 163679 203614
| A. | 在强碱溶液中:Na+.K+.AlO2-.CO32- | |
| B. | 在含大量Fe3+的溶液中:NH4+.Na+.Cl-.SCN- | |
| C. | 在c(H+)=10-13mol/L 的溶液中:NH4+.Al3+.SO42-.NO3- | |
| D. | 在pH=1的溶液中:K+.Fe2+.Cl-.NO3- |


 和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式
和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式 +4Cu(OH)2+2NaOH$\stackrel{△}{→}$NaOOC-COONa+2Cu2O↓+6H2O.
+4Cu(OH)2+2NaOH$\stackrel{△}{→}$NaOOC-COONa+2Cu2O↓+6H2O. 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示: