8.常温下,在pH=1的某溶液中可能有Na+、Fe2+、Fe3+、I-、Cl-、CO32-中的几种,现取100mL,该溶液进行如下实验,根据实验结果,下列判断正确的是( )


| A. | Fe2+、I-、Cl-三种离子一定存在 | |
| B. | CO32-一定不存在,不能确定Na+和Cl-是否存在 | |
| C. | Fe3+与Fe2+至少有一种 | |
| D. | 该溶液中c(Cl-)至少为0.2mol•L-1 |
7.下列物质的名称或化学式与颜色不一致的是( )
| A. | S(淡黄色) | B. | NO(无色) | C. | 无水硫酸铜(蓝色) | D. | NO2(红棕色) |
5.某有机物结构简式如图所示,下列有关该有机物叙述正确的是( )


| A. | 该有机物分子式为C 9H 8O 3 | |
| B. | 该有机物可以和氯化铁溶液发生显色反应 | |
| C. | 1 mo1该有机物与溴水反应,最多消耗2 mol Br 2 | |
| D. | 1 mol该有机物最多与2 mol NaOH反应 |
4.N A表示阿伏加德罗常数的值,下列判断正确的是( )
| A. | 标准状况下,2.24 L 16O 2和3.6 g 18O 2均含有0.2N A个氧原子 | |
| B. | 1.7 g H 218O 2中含有的电子数为0.9 N A | |
| C. | 电解精炼铜时,若阴极得到N A个电子,则阳极质量减少32g | |
| D. | 标准状况下,2.24 L甲烷、戊烷混合物所含分子数为0.1N A |
3.一些烷烃的燃烧热(KJ/mol)如表:下列表达正确的是( )
| 化合物 | 燃烧热 | 化合物 | 燃烧热 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
| A. | 稳定性:正丁烷>异丁烷 | |
| B. | 乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=-1560.8KJ/mol | |
| C. | 正戊烷的燃烧热大约在3540 KJ/mol左右 | |
| D. | 相同质量的烷烃,碳的质量分数越大,完全燃烧放出的热量越多 |
2.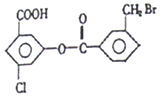 某有机物的结构简式如图:1mol该有机物与足量的氢氧化钠溶液混合并共热,
某有机物的结构简式如图:1mol该有机物与足量的氢氧化钠溶液混合并共热,
充分反应后最多可消耗氢氧化钠的物质的量为( )
 某有机物的结构简式如图:1mol该有机物与足量的氢氧化钠溶液混合并共热,
某有机物的结构简式如图:1mol该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为( )
| A. | 4mol | B. | 5mol | C. | 6mol | D. | 7mol |
1.设 NA 表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,22.4LCH4 和 CH2C12 的混合物所含有的分子数目为 NA | |
| B. | 3g 的甲基中含有的电子数为 1.6NA | |
| C. | 0.5mol 的有机物 C15H32 中含有的共价键数日为 24NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共 14g,其原子数为 3NA |
20.海水资源的综合利用十分重要,不需要通过化学变化就能够从海水中获得的物质是( )
0 163300 163308 163314 163318 163324 163326 163330 163336 163338 163344 163350 163354 163356 163360 163366 163368 163374 163378 163380 163384 163386 163390 163392 163394 163395 163396 163398 163399 163400 163402 163404 163408 163410 163414 163416 163420 163426 163428 163434 163438 163440 163444 163450 163456 163458 163464 163468 163470 163476 163480 163486 163494 203614
| A. | 食盐 | B. | 钠 | C. | 溴 | D. | 碘 |
 +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3; +2H2O.
+2H2O.