题目内容
在2 L密闭容器中加入或通入一定量A、B、C三种物质,在一定条件下发生反应(如图1),3 min后给体系加热,气体C的体积分数φ(C)和混合气体的平均相对分子质量Mr均随温度发生了图示变化(如图2,图3)。下列有关说法不正确的是( ) 
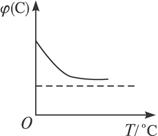
图1 图2

图3
A.前2 min C的平均反应速率为1 mol·L-1·min-1
B.该反应的化学方程式为:2A+B![]() 2C
2C
C.正反应是放热反应
D.A、B一定均为气态
D
解析:根据反应方程式中各物质变化的物质的量之比等于化学计量数之比,由图1可判断出该反应的化学方程式为:2A+B![]() 2C。前2 min C的平均反应速率为
2C。前2 min C的平均反应速率为![]() =1mol·L-1·min-1。由图2可知,随着温度的升高,C的体积分数降低,即平衡逆向移动,故正反应是放热反应。由图3可知,随着温度的升高,平衡逆向移动,混合气体的平均相对分子质量
=1mol·L-1·min-1。由图2可知,随着温度的升高,C的体积分数降低,即平衡逆向移动,故正反应是放热反应。由图3可知,随着温度的升高,平衡逆向移动,混合气体的平均相对分子质量![]() 减小。当A、B都为气态时,平衡逆向移动,气体的质量不变,但气体的物质的量增多,故混合气体的平均相对分子质量减小。当A为气态、B不为气态时,平衡逆向移动,气体的质量减小,但气体的物质的量不变,故混合气体的平均相对分子质量也减小。
减小。当A、B都为气态时,平衡逆向移动,气体的质量不变,但气体的物质的量增多,故混合气体的平均相对分子质量减小。当A为气态、B不为气态时,平衡逆向移动,气体的质量减小,但气体的物质的量不变,故混合气体的平均相对分子质量也减小。

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
 GC2(g) ΔH1=-296 KJ·mol-1,2GC3(g)
GC2(g) ΔH1=-296 KJ·mol-1,2GC3(g)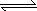 2GC2(g)+C2(g) ΔH2=+198 KJ·mol-1
2GC2(g)+C2(g) ΔH2=+198 KJ·mol-1 2GC3(g) ΔH3=________.
2GC3(g) ΔH3=________. 2GC3(g) ΔH=a KJ·mol-1图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.
2GC3(g) ΔH=a KJ·mol-1图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.

 2SO3(g)
ΔH <0,n(O2)随时间的变化如图实线所示:
2SO3(g)
ΔH <0,n(O2)随时间的变化如图实线所示: