题目内容
对于反应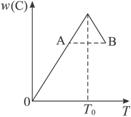
(1)T0对应的v(正)与v(逆)的关系是_______________。
(2)正反应为热反应_______________。
(3)A、B两点正反应速率的大小关系是_______________。
(4)温度T<T0时,w(C)逐渐增大的原因是______________________________。
解析:(1)T0对应的点恰好达到平衡,所以,v(正)=v(逆)。(2)随着温度的升高,C的质量分数反而下降,说明正反应为放热反应。(3)B点比A点温度高,所以,v(B)>v(A)。(4)温度T<T0时,由于反应还没有达到平衡,所以,随着温度的升高,w(C)逐渐增大。
答案:(1)v(正)=v(逆)
(2)放
(3)v(B)>v(A)
(4)反应未达到平衡,随着温度的升高,w(C)逐渐增大

练习册系列答案
相关题目
下列说法不正确的是( )
| A.MnO2能加速H2O2的分解,是因为MnO2可以降低反应所需的活化能 |
| B.向橙色的K2Cr2O7溶液中滴加NaOH溶液,溶液颜色变黄,说明化学平衡发生了移动 |
| C.将NO2和N2O4混合气体的平衡体系加压,容器内气体颜色变深,这一事实不能用勒夏特列原理解释 |
D.在密闭容器中,对于反应2A(g)+B(g) 2C(g),增大压强后,平衡混合气的平均相对分子质量减小 2C(g),增大压强后,平衡混合气的平均相对分子质量减小 |
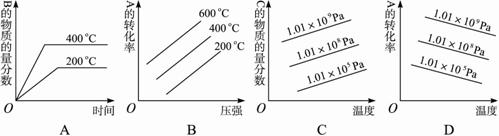
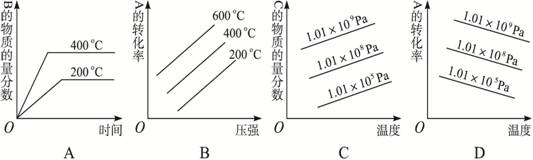
 2C(g)+Q (Q>0),下列图象正确的是
?
2C(g)+Q (Q>0),下列图象正确的是
?