题目内容
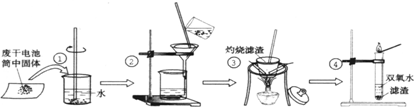
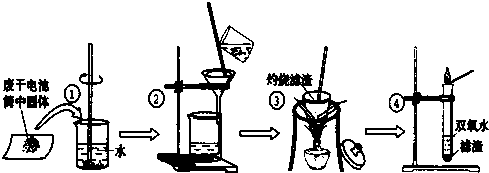
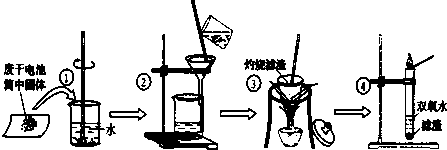
某同学用废干电池内的黑色固体(可能含有MnO2、NH4Cl、ZnCl2等物质)进行如图所示实验: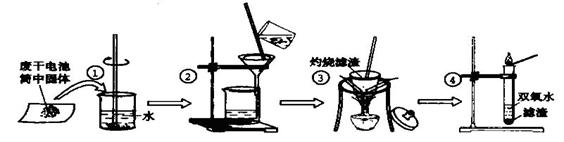
(1)操作②中过滤时玻璃棒的作用: ;
(2)操作④加入③中所得滤渣,试管中迅速产生能使带火星的木条复燃的气体,由此推测滤渣含有MnO2,试管中发生反应的化学方程式: ;
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的物质为: 。
(4)已知氯化锌与稀氨水反应先生成Zn(OH)2白色沉淀,Zn(OH)2可以溶于稀氨水生成可溶性的Zn(NH3)4(OH)2;下列是该同学对操作②的滤液主次成分进行探究的过程:
(一)[猜想I]:主要成分为氯化铵;
[验证(操作)过程]:取少量滤液加入NaOH固体,并加热;
[实验现象]:闻到有轻微的氨味;
[判断猜想]: (填“猜想I成立”或“猜想I不成立”);
(二)[猜想II]:主要成分为氯化锌;
[验证(操作)过程]: ;
[实验现象]: ;
[判断猜想]:猜想Ⅱ成立;
由上述实验得出的结论是:滤液中的主次成分: 。
(1)引流作用(2分)
(2) 2H2O2 == 2H2O + O2↑(2分)
(3) 炭(或碳、或C) (2分)
(4)(一)[判断猜想]:猜想I不成立 (2分)
(二)[验证(操作)过程]:取少量滤液逐滴滴入稀氨水(2分)
[实验现象]:先有白色沉淀、滴入过量稀氨水后白色沉淀溶解(2分);
[判断猜想]:结论:主要为氯化锌,其中含少量的氯化铵(2分)。
[若说成氯化铵和氯化锌的混合物给1分;若说成只有氯化锌没有氯化铵0分]