题目内容
甲酸(CH2O2),俗称蚁酸,结构式为:
某化学兴趣小组的同学在分析甲酸的组成和结构后,对甲酸的性质提出如下猜想并设计了相关实验加以验证:
猜想I:甲酸具有酸性;
实验I:在甲酸溶液中滴加紫色石蕊试液;
猜想II:甲酸能发生银镜反应;
实验II:(步骤如图所示);
回答下列问题:
(1 )请你再设计出至少2个实验方案来验证甲酸的酸性:______、______;
(2)请你进一步设计实验方案证明甲酸是弱酸:______;
(3)依如图所示的实验,加热20分钟后并没有出现预期的实验现象.该小组同学预期的化学反应是(用化学方程式表示)______,请你从理论上简单解释实验中没有出现该现象的原因______;
(4)在仔细分析甲酸分子组成元素的基础上,请你再提出一个甲酸在浓硫酸作用下可能具有的性质的猜想是______.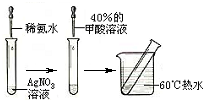
某化学兴趣小组的同学在分析甲酸的组成和结构后,对甲酸的性质提出如下猜想并设计了相关实验加以验证:
猜想I:甲酸具有酸性;
实验I:在甲酸溶液中滴加紫色石蕊试液;
猜想II:甲酸能发生银镜反应;
实验II:(步骤如图所示);
回答下列问题:
(1 )请你再设计出至少2个实验方案来验证甲酸的酸性:______、______;
(2)请你进一步设计实验方案证明甲酸是弱酸:______;
(3)依如图所示的实验,加热20分钟后并没有出现预期的实验现象.该小组同学预期的化学反应是(用化学方程式表示)______,请你从理论上简单解释实验中没有出现该现象的原因______;
(4)在仔细分析甲酸分子组成元素的基础上,请你再提出一个甲酸在浓硫酸作用下可能具有的性质的猜想是______.

(1)根据酸的通性分析,甲酸呈酸性,则在溶液中电离出氢离子,用PH试纸检验变红色,能与碱发生中和反应,能与碳酸盐反应生成二氧化碳气体,
故答案为:测定pH或滴加Na2CO3溶液、或将甲酸滴加到滴有酚酞的NaOH溶液中;
(2)如甲酸为弱酸,则其钠盐溶液水解呈碱性,将等pH的HCOOH溶液和HCl溶液稀释相同倍数时,PH变化不同,强酸PH变化较大,弱酸PH变化较小,溶液的导电性不同,
故答案为:测定HCOONa溶液的pH;或将等pH的HCOOH溶液和HCl溶液稀释相同倍数,测其pH的变化;或比较等浓度甲酸和盐酸的导电性等;
(3)甲酸的结构为
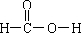
,分子中含有醛基、羧基、羰基和羟基,应具有还原性和酸性等性质,理论上甲酸的醛基被氧化成羧基,甲酸变成碳酸.碳酸不稳定分解成二氧化碳和水,反应方程式为:HCOOH+2Ag(NH3)2OH
2H2O+2Ag+4NH3↑+CO2 ↑,实验Ⅱ中没有出现预期的现象的可能原因是羟基的影响,另外进行银镜反应时,须在碱性条件下反应,如稀氨水量不足,则无银镜产生,
故答案为:HCOOH+2Ag(NH3)2OH
2H2O+2Ag+4NH3↑+CO2 ↑;由于羟基对醛基的影响,导致甲酸中的醛基不具有典型醛基的性质;羧基中C原子和2个O原子之间形成1个大л键,而使甲酸分子中的醛基性质不太典型;或答稀氨水量不足,使甲酸与银氨溶液混合后仍显酸性;
(4)根据浓硫酸具有脱水性,以及甲酸的分子式为CH2O2,根据质量守恒可推测甲酸在浓硫酸的作用下脱水生成CO和H2O,故答案为:甲酸在浓硫酸的作用下脱水生成CO和H2O;
故答案为:测定pH或滴加Na2CO3溶液、或将甲酸滴加到滴有酚酞的NaOH溶液中;
(2)如甲酸为弱酸,则其钠盐溶液水解呈碱性,将等pH的HCOOH溶液和HCl溶液稀释相同倍数时,PH变化不同,强酸PH变化较大,弱酸PH变化较小,溶液的导电性不同,
故答案为:测定HCOONa溶液的pH;或将等pH的HCOOH溶液和HCl溶液稀释相同倍数,测其pH的变化;或比较等浓度甲酸和盐酸的导电性等;
(3)甲酸的结构为
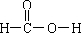
,分子中含有醛基、羧基、羰基和羟基,应具有还原性和酸性等性质,理论上甲酸的醛基被氧化成羧基,甲酸变成碳酸.碳酸不稳定分解成二氧化碳和水,反应方程式为:HCOOH+2Ag(NH3)2OH
| 水浴 |
故答案为:HCOOH+2Ag(NH3)2OH
| 水浴 |
(4)根据浓硫酸具有脱水性,以及甲酸的分子式为CH2O2,根据质量守恒可推测甲酸在浓硫酸的作用下脱水生成CO和H2O,故答案为:甲酸在浓硫酸的作用下脱水生成CO和H2O;

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
布尔津县夏天蚊子特别多,被蚊子叮咬后人会感觉痛痒,这是由于蚊子分泌出的酸性物质有刺激作用,该酸性物质的主要成分是甲酸(CH2O2)。下列有关说法正确的是( )
| A.甲酸溶液能使紫色石蕊试液变蓝色 |
| B.甲酸中碳、氢、氧三种元素的质量比为6:1:16 |
| C.甲酸由1个碳原子、2个氢原子和2氧原子构成 |
| D.可选用浓氢氧化钠溶液等碱性物质来涂抹患处 |
 (2009?汕头二模)甲酸(CH2O2),俗称蚁酸,结构式为:
(2009?汕头二模)甲酸(CH2O2),俗称蚁酸,结构式为:


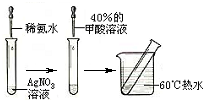 甲酸(CH2O2),俗称蚁酸,结构式为:
甲酸(CH2O2),俗称蚁酸,结构式为: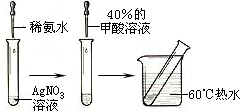 甲酸(CH2O2),俗称蚁酸,结构式为:______.某化学兴趣小组的同学在分析甲酸的组成和结构后,对甲酸的性质提出如下猜想并设计了相关实验加以验证:
甲酸(CH2O2),俗称蚁酸,结构式为:______.某化学兴趣小组的同学在分析甲酸的组成和结构后,对甲酸的性质提出如下猜想并设计了相关实验加以验证: