��Ŀ����
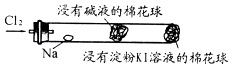
����Ŀ��ijѧ��������ͼ��ʾװ�öԵ������Һ�����Խ���ʵ��̽��������˵������ȷ���ǣ�������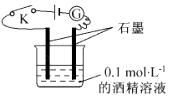
A.�պϿ���K������ ![]() ָ�벻����ƫת��֤���ƾ���Һ�Ƿǵ����
ָ�벻����ƫת��֤���ƾ���Һ�Ƿǵ����
B.�պϿ��أ�����Һ��ͨ����������������ͨ�룬������ʾ�����������ǵ����
C.ȡ��0.1 molL��1��������Һ�滻�ƾ���Һ�������Ƶ�ʾ����ͬ��˵�������Ƿǵ����
D.�պϿ��أ����ձ��м�NaCl���壬��Ȼ�����ܽ⣬���ڲ���Ӧ���ʵ�����ָ�벻����ƫת
���𰸡�C
��������A��������K�պϺ�����ָ�벻����ƫת��˵�������γɱպϻ�·��֤���ƾ���Һ�����磬�ƾ��Ƿǵ���ʣ�A���������⣻
B���պϿ���K������Һ��ͨ��������������ˮ��Ӧ��������ʹ����ᣬ�������������������ӣ���������ͨ�룬����Ũ������������ǿ��������ʾ�����������ǵ��ʣ�����������������ԭ�ʣ����Բ��ܵó������ǵ���ʵĽ��ۣ����������ǵ����Ҳ���Ƿǵ���ʣ�B���������⣻
C��ȡ��0.1 molL��1��������Һ�滻�ƾ���Һ�������Ƶ�ʾ����ͬ��˵�������γɱպϻ�·��֤��������Һ�����磬����Ϊ������Һ��ֻ���ڷ��ӣ������ǻ������Ҳ��ܵ��룬�������Ƿǵ���ʣ�C�������⣻
D���պϿ���K�����ձ��м���NaCl���壬�Ȼ�������ˮ��������������ӣ������Һ�ܵ��磬���Ե�����ָ�뷢��ƫת��D���������⣮
�ʴ�Ϊ��C��
�����ɵ���Ϊ�����ƶ����ӵĻ�����Ϊ����ʡ�A���ƾ���Һ�����磬�ƾ��������Ƿǵ���ʣ�B�������ǵ��ʼ����ǵ����Ҳ���Ƿǵ���ʣ�C�����Dz��ܵ��룬�Ƿǵ���ʣ�D�����������ˮ��������������ӣ������Һ�ܵ��磮

 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д�����Ŀ��ͨ�����ǰѲ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�ķ�Ӧ�ȵ��ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
��ѧ�� | Si��O | Si��Cl | H��H | H��Cl | Si��Si | Si��C |
����/kJmol��1 | 460 | 360 | 436 | 431 | 176 | 347 |
��ش��������⣺
��1����֪Si��SiC��SiO2�ۻ�ʱ�������������ѧ�����Ƚ������������ʵ��۵�ߵͣ��������������SiCSi��SiSiO2
��2����ҵ�ϸߴ����ͨ�����з�Ӧ��ȡ��
SiCl4��g��+2H2��g�� ![]() Si��s��+4HCl��g����
Si��s��+4HCl��g����
��2mol H2���ɸߴ�����������ա��ų���������kJ��