题目内容
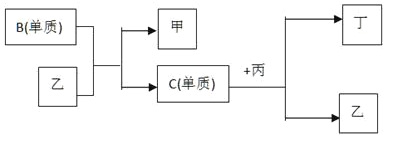
【题目】有关物质的转化关系如图所示(部分物质与条件己略去)。已知A、C是由两种相同元素组成的物质,其中A的摩尓质量为65g·mol-1,C是白色粉末且焰色反应呈黄色,I是最常见的液体,E是一种红棕色气体,B、F都是无色气体单质。请回答下列问题:

(1)K的电子式为:___________________________。
(2)E的化学式为:___________________________。
(3)写出反应①的化学方程式:___________________________。
(4)写出反应②的离子方程式:________________________。
【答案】![]() NO2 3NaN3
NO2 3NaN3 ![]() Na3N + 4N2↑ 3NO2 + H2O = 2H+ + 2NO3-+ NO
Na3N + 4N2↑ 3NO2 + H2O = 2H+ + 2NO3-+ NO
【解析】
I是最常见的液体,E是一种红棕色气体,可知I为水,E为二氧化氮,二氧化氮与水反应生成一氧化氮(D)和硝酸(J),B、F都是无色气体单质,B为氮气,K为氨气,C是白色粉末且焰色反应呈黄色,为含有钠元素和氮元素的化合物,其与A物质组成元素相同,已知A摩尔质量为65g·mol-1,可以推知化合物A为NaN3,根据氧化还原反应规律,由于B为氮气,为氧化产物,所以C为还原产物,氮元素价态降低,所以C为Na3N。
(1)根据以上分析可知K为氨气,其电子式为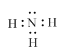 ,
,
故答案为: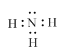 ;
;
(2)根据以上分析可知E为二氧化氮,化学式为NO2,
故答案为:NO2;
(3)反应①为NaN3受到撞击后分解为氮气和Na3N,化学方程式为3NaN3 ![]() Na3N + 4N2↑,
Na3N + 4N2↑,
故答案为:3NaN3 ![]() Na3N + 4N2↑;
Na3N + 4N2↑;
(4)反应②为二氧化氮与水反应生成一氧化氮和硝酸,所以离子方程式为3NO2 + H2O = 2H+ + 2NO3-+ NO,
故答案为:3NO2 + H2O = 2H+ + 2NO3-+ NO。

 口算能手系列答案
口算能手系列答案