题目内容
实验室中有一瓶氯化钾和氯化钙的固体混和物,通过下面的实验除去氯化钾中氯化钙,并利用纯净的氯化钾配制一定浓度的氯化钾溶液.根据实验步骤填写下列空白.

回答下列问题
(1)加入的A是________.(填分子式,下同)
(2)操作②的名称是________.操作①、②均要用到的玻璃仪器有________.
(3)B物质是________,加入过量的B反应的离子方程式为________.
(4)称取一定量纯净的KCl,配制一定浓度的氯化钾溶液.
(ⅰ)某同学用托盘天来称取一定质量的KCl,称法如下图所示,天平的指针在标尺中间.此操作是否正确________(填正确或不正确);若按此操作称量,所称KCl的实际质量为________g (已知烧杯的质量为12.9克).

(ⅱ)某学生将准确称量的KCl固体放入烧杯中,加入约30毫升蒸馏水,用玻璃棒搅拌使其溶解.将溶液由烧杯倒入100毫升容量瓶中,然后往容量瓶中小心地加蒸馏水,直到液面接近刻度1-2厘米处,改用胶头滴管加蒸馏水,使溶液凹面最低点恰好与刻度相切,把容量瓶盖紧,再振荡摇匀.该生操作中的错误是________和________.
解析:
(1)K2CO3.
(2)蒸发.玻璃棒.
(3)HCl,2H++CO32-=H2O+CO2↑.
(4)(ⅰ)不正确,14.5 g.
(ⅱ)没有用玻璃棒引流和烧杯和玻璃棒没有洗涤.

实验室中有一瓶氯化钾和氯化钙的固体混和物,通过下面的实验可制得纯净的氯化钾。根据实验步骤填写下列空白。
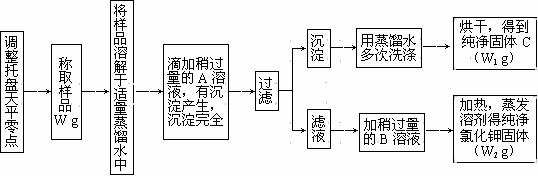 |
⑴ 加入的A是 ,检验A是否过量的方法是 。
⑵ 除烧杯、漏斗外,上述实验中的过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
⑶ 滤液中加入的B物质是 。应该加入过量的B物质,理由是 。
⑷ 得到的固体C是 。
⑸ 为检验提纯的KCl的纯度,需配制500 mL4.00 mol·L-1KCl(纯KCl)溶液,所用的定量仪器除天平、量筒外还有 (填仪器名称),需要KCl固体 g。
⑹ 若要确定该混和物中氯化钾和氯化钙的质量比,需要用到上述实验数据中的 w g和 。