题目内容
(2013?丰台区二模)工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下: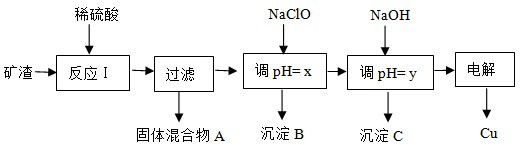
已知:Cu2O+2H+=Cu+Cu2++H2O
(1)固体混合物A中的成分是
(2)反应Ⅰ完成后,铁元素的存在形式为
请写出生成该离子的离子方程式
(3)x、y对应的数值范围分别是
(4)电解法获取Cu时,阴极反应式为
(5)下列关于NaClO调pH的说法正确的是
a.加入NaClO可使溶液的pH降低
b.NaClO能调节pH的主要原因是由于发生反应ClO-+H+?HClO,ClO-消耗H+,从而达到调节pH的目的
c.NaClO能调节pH的主要原因是由于NaClO水解ClO-+H2O?HClO+OH-,OH-消耗H+,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为

已知:Cu2O+2H+=Cu+Cu2++H2O
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
| 沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
SiO2、Cu
SiO2、Cu
.(2)反应Ⅰ完成后,铁元素的存在形式为
Fe2+
Fe2+
.(填离子符号)请写出生成该离子的离子方程式
2Fe3++Cu=Cu2++2Fe2+
2Fe3++Cu=Cu2++2Fe2+
.(3)x、y对应的数值范围分别是
3.2≤pH<4.0
3.2≤pH<4.0
、5.2≤pH<5.4
5.2≤pH<5.4
.(4)电解法获取Cu时,阴极反应式为
Cu2++2e-=Cu
Cu2++2e-=Cu
,阳极反应式为2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.(5)下列关于NaClO调pH的说法正确的是
b
b
.a.加入NaClO可使溶液的pH降低
b.NaClO能调节pH的主要原因是由于发生反应ClO-+H+?HClO,ClO-消耗H+,从而达到调节pH的目的
c.NaClO能调节pH的主要原因是由于NaClO水解ClO-+H2O?HClO+OH-,OH-消耗H+,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为
5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO
5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO
.分析:(1)固体混合物是不溶于稀硫酸的物质,根据反应:Cu2O+2H+=Cu+Cu2++H2O,得出A的成分是SiO2、Cu;
(2)由于单质铜存在,铁元素以Fe2+形式存在,反应方程式:2Fe3++Cu=Cu2++2Fe2+;
(3)根据氢氧化铁和氢氧化铝开始沉淀和沉淀结束的PH关系,x范围是:3.2≤pH<4.0,目的是沉淀氢氧化铁;y范围是:5.2≤pH<5.4,沉淀氢氧化铝;
(4)电解法获取Cu时,阴极发生还原反应:Cu2++2e-=Cu;阳极发生氧化反应:2Cl--2e-=Cl2↑;
(5)a、次氯酸钠中的次氯酸根结合溶液中的氢离子,PH升高;
b、NaClO能调节pH的主要原因是由于发生反应ClO-+H+?HClO,ClO-消耗H+,从而达到调节pH的目的;
c、溶液显示酸性,次氯酸是弱酸,次氯酸根结合酸溶液中的氢离子;
(6)生成一种具有漂白作用的物质是次氯酸.
(2)由于单质铜存在,铁元素以Fe2+形式存在,反应方程式:2Fe3++Cu=Cu2++2Fe2+;
(3)根据氢氧化铁和氢氧化铝开始沉淀和沉淀结束的PH关系,x范围是:3.2≤pH<4.0,目的是沉淀氢氧化铁;y范围是:5.2≤pH<5.4,沉淀氢氧化铝;
(4)电解法获取Cu时,阴极发生还原反应:Cu2++2e-=Cu;阳极发生氧化反应:2Cl--2e-=Cl2↑;
(5)a、次氯酸钠中的次氯酸根结合溶液中的氢离子,PH升高;
b、NaClO能调节pH的主要原因是由于发生反应ClO-+H+?HClO,ClO-消耗H+,从而达到调节pH的目的;
c、溶液显示酸性,次氯酸是弱酸,次氯酸根结合酸溶液中的氢离子;
(6)生成一种具有漂白作用的物质是次氯酸.
解答:解:(1)加入硫酸发生了反应:Cu2O+2H+=Cu+Cu2++H2O,故固体A的成分是二氧化硅和铜,故答案为:SiO2、Cu;
(2)由于发生了反应,2Fe3++Cu=Cu2++2Fe2+,溶液中铁元素的存在形式为:Fe2+;
故答案为:Fe2+;2Fe3++Cu=Cu2++2Fe2+
(3)调节PH=x,目的是生成沉淀氢氧化铁,PH应该大于3.2,小于4.0;调节PH=y,生成沉淀氢氧化铝,PH需要大于5.2,小于5.4;
故答案为:3.2≤pH<4.0;5.2≤pH<5.4;
(4)电解法获取Cu时,阴极铜离子得到电子,反应为:Cu2++2e-=Cu;阳极发生氧化反应,2Cl--2e-=Cl2↑;
故答案为:Cu2++2e-=Cu;2Cl--2e-=Cl2↑
(5)a、加入NaClO可使溶液的pH会升高,因为次氯酸根消耗了溶液中的氢离子,故a错误;
b、由于NaClO能调节pH的主要原因是由于发生反应ClO-+H+?HClO,ClO-消耗H+,故b正确;
c、次氯酸钠调节溶液的PH,不是水解,是次氯酸根结合溶液中的氢离子,氢离子浓度下降,PH升高,故c错误;
故选b;
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式是:5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO;
故答案为:5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO.
(2)由于发生了反应,2Fe3++Cu=Cu2++2Fe2+,溶液中铁元素的存在形式为:Fe2+;
故答案为:Fe2+;2Fe3++Cu=Cu2++2Fe2+
(3)调节PH=x,目的是生成沉淀氢氧化铁,PH应该大于3.2,小于4.0;调节PH=y,生成沉淀氢氧化铝,PH需要大于5.2,小于5.4;
故答案为:3.2≤pH<4.0;5.2≤pH<5.4;
(4)电解法获取Cu时,阴极铜离子得到电子,反应为:Cu2++2e-=Cu;阳极发生氧化反应,2Cl--2e-=Cl2↑;
故答案为:Cu2++2e-=Cu;2Cl--2e-=Cl2↑
(5)a、加入NaClO可使溶液的pH会升高,因为次氯酸根消耗了溶液中的氢离子,故a错误;
b、由于NaClO能调节pH的主要原因是由于发生反应ClO-+H+?HClO,ClO-消耗H+,故b正确;
c、次氯酸钠调节溶液的PH,不是水解,是次氯酸根结合溶液中的氢离子,氢离子浓度下降,PH升高,故c错误;
故选b;
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式是:5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO;
故答案为:5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO.
点评:本题考查了利用矿渣提取铜的操作,涉及的内容较多,难度较大,需要充分利用所学知识及题中信息.

练习册系列答案
相关题目