题目内容
3.已知断开1mol N≡N键需要946kJ的能量,断开1mol H-H键需要436kJ的能量,生成1mol N-H键放出391kJ的能量,试计算生成2mol NH3时会放出(填“放出”或“吸收”)92kJ能量.分析 化学反应中,化学键断裂吸收能量,形成新化学键放出能量,反应热=吸收的总能量-放出的总能量,据此计算出生成2mol氨气的反应热.
解答 解:反应热=化学键断裂吸收的总能量-化学键形成放出的总能量,所以生成2molNH3的反应热=946kJ+3×436 kJ-2×3×391kJ=-92kJ,所以生成2mol氨气放出92kJ的热量;由于N2和H2生成NH3的反应为可逆反应,1mol N2和3mol H2不能完全反应生成2molNH3,所以反应放出的热量小于92kJ,
故答案为:放出;92.
点评 本题考查反应热的计算,题目难度中等,注意把握从键能的角度计算反应热的方法,明确“反应热=化学键断裂吸收的总能量-化学键形成放出的总能量”是解答本题关键.

练习册系列答案
相关题目
14.不能与BaCl2溶液形成沉淀的试剂有( )
| A. | NaCl溶液 | B. | Na2CO3溶液 | C. | Na2SO4溶液 | D. | AgNO3溶液 |
18.用有机物甲可制备环己二烯( ),其反应路线如图所示,下列有关判断正确的是( )
),其反应路线如图所示,下列有关判断正确的是( )
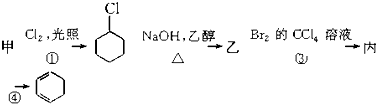
 ),其反应路线如图所示,下列有关判断正确的是( )
),其反应路线如图所示,下列有关判断正确的是( )
| A. | 甲的化学名称是苯 | |
| B. | 乙的结构简式为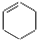 | |
| C. | 反应①为加成反应 | |
| D. | 有机物丙既能发生加成反应,又能发生取代反应 |
15.下列各组物质中,互为同分异构体的是( )
| A. | 果糖 葡萄糖 | B. | 蔗糖 葡萄糖 | C. | 淀粉 纤维素 | D. | 乙酸 乙醇 |
12.由-C6H5、-C6H4-、-CH2-、-OH四种原子团各一种组成属于酚类的物质的种类有( )
| A. | 3种 | B. | 4种 | C. | 1种 | D. | 2种 |
18.某烃含碳、氢元素的质量比为6:1,该径对氮气的相对密度为2,它即可使溴水褪色,又能与氢气加成,而与氢气的加成产物的有3种同分异构体,该径可以是( )
| A. | H2C=CH-CH2-CH3 | B. | 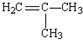 | C. | H2C=CH2 | D. | 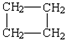 |