题目内容
某元素R的气态氢化物为HXR,且R在该氢化物中的质量分数为94%,8.5g的HXR气体在标准状态下的体积是5.6L。则HXR的相对分子量为 ;HXR的化学式为 。
34 H2S
5.6L在标准状况下的物质的量是5.6L÷22.4L/mol=0.25mol,所以HXR的相对分子质量是8.5÷0.25=34。根据R元素的含量可知,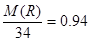 ,解得M(R)=32,则x=2,所以化学式为H2S。
,解得M(R)=32,则x=2,所以化学式为H2S。
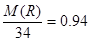 ,解得M(R)=32,则x=2,所以化学式为H2S。
,解得M(R)=32,则x=2,所以化学式为H2S。
练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目