题目内容
(2012?浙江)甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整.向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
回答下列问题:
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H=
(2)在初始阶段,甲烷蒸汽重整的反应速率
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应CH4(g)+H2O(g)?CO(g)+3H2(g)的KP=
;随着温度的升高,该平衡常数
(4)从能量角度分析,甲烷自热重整方法的先进之处在于
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如图1、图2:

①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是
A.600℃,0.9MpaB.700℃,0.9MPaC.800℃,1.5MpaD.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图(如图3):
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是
| 反应过程 | 化学方程式 | 焓变△H(kJ/mol) | 活化能Ea(kJ/mol) |
| 甲烷氧化 | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 蒸汽重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 | 240.1 |
| CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 | 243.9 |
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H=
-41.2
-41.2
kJ/mol.(2)在初始阶段,甲烷蒸汽重整的反应速率
小于
小于
甲烷氧化的反应速率(填大于、小于或等于).(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应CH4(g)+H2O(g)?CO(g)+3H2(g)的KP=
| p3(H2)?P(CO) |
| P(CH4)?P(H2O) |
| p3(H2)?P(CO) |
| P(CH4)?P(H2O) |
增大
增大
(填“增大”、“减小”或“不变”).(4)从能量角度分析,甲烷自热重整方法的先进之处在于
放热的甲烷氧化反应为吸热的蒸气重整提供能量
放热的甲烷氧化反应为吸热的蒸气重整提供能量
.(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如图1、图2:

①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是
B
B
.A.600℃,0.9MpaB.700℃,0.9MPaC.800℃,1.5MpaD.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图(如图3):
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是
导致生成的氢气和氧气反应
导致生成的氢气和氧气反应
.分析:(1)根据盖斯定律,由蒸汽重整的两个反应CH4(g)+2H2O(g)=CO2(g)+4H2(g)减CH4(g)+H2O(g)=CO(g)+3H2(g),可得反应:CO(g)+H2O(g)=CO2(g)+H2(g),据此计算反应热;
(2)由表中数据可知,甲烷氧化的活化能低于蒸气重整的活化能,活化能越低,反应速率越快;
(3)根据平衡常数k的表达式,利用信息直接书写Kp;
该反应为吸热反应,升高温度,平衡向正反应移动,平衡常数增大;
(4)从能量的角度分析,放热的甲烷氧化反应为吸热的蒸气重整提供能量;
(5)①根据图象中,温度、压强对H2和CO物质的量分数的影响数据,选择判断;
②结合图象可知在600℃、0.1 MPa的条件下,平衡时系统中H2的物质的量分数达到70%,起始进料时H2的物质的量分数为0,据此可画出H2的物质的量分数随时间变化的示意图;
(6)如果反应过程中进氧气的量过大,会导致生成的氢气和氧气反应,导致质量分数降低.
(2)由表中数据可知,甲烷氧化的活化能低于蒸气重整的活化能,活化能越低,反应速率越快;
(3)根据平衡常数k的表达式,利用信息直接书写Kp;
该反应为吸热反应,升高温度,平衡向正反应移动,平衡常数增大;
(4)从能量的角度分析,放热的甲烷氧化反应为吸热的蒸气重整提供能量;
(5)①根据图象中,温度、压强对H2和CO物质的量分数的影响数据,选择判断;
②结合图象可知在600℃、0.1 MPa的条件下,平衡时系统中H2的物质的量分数达到70%,起始进料时H2的物质的量分数为0,据此可画出H2的物质的量分数随时间变化的示意图;
(6)如果反应过程中进氧气的量过大,会导致生成的氢气和氧气反应,导致质量分数降低.
解答:解:(1)根据盖斯定律,由蒸汽重整的两个反应CH4(g)+2H2O(g)=CO2(g)+4H2(g)减CH4(g)+H2O(g)=CO(g)+3H2(g),可得反应:CO(g)+H2O(g)=CO2(g)+H2(g),故△H=165.0kJ/mol-206.2kJ/mol=-41.2kJ/mol,
故答案为:-41.2;
(2)由表中数据可知,甲烷氧化的活化能低于蒸气重整的活化能,活化能越低,反应速率越快,故初始阶段,甲烷蒸汽重整的反应速率小于甲烷氧化的反应速率,故答案为:小于;
(3)根据平衡常数k的表达式,可知反应CH4(g)+H2O(g)?CO(g)+3H2(g)的KP=
,
该反应为吸热反应,升高温度,平衡向正反应移动,平衡常数增大,
故答案为:
,增大;
(4)从能量的角度分析,甲烷自热重整方法的先进之处在于:放热的甲烷氧化反应为吸热的蒸气重整提供能量,提高能源的利用率,故答案为:放热的甲烷氧化反应为吸热的蒸气重整提供能量;
(5)①由图中数据可知,0.9 MPa时,H2的物质的量分数>65%,CO物质的量分数<10%,则700℃符合,1.5 MPa时,H2的物质的量分数>65%,CO物质的量分数<10%,则温度要高于750℃,低于约725℃,矛盾,故B正确,ACD错误,故答案为:B;
②起始进料时H2的物质的量分数为0,结合图象可知600℃,0.1 MPa的条件下,平衡时系统中H2的物质的量分数达到70%,据此画出H2的物质的量分数随时间变化的示意图为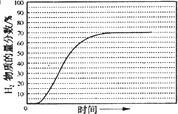 ,
,
故答案为: ;
;
(6)如果反应过程中进氧气的量过大,会导致生成的氢气和氧气反应,导致质量分数降低,
故答案为:导致生成的氢气和氧气反应.
故答案为:-41.2;
(2)由表中数据可知,甲烷氧化的活化能低于蒸气重整的活化能,活化能越低,反应速率越快,故初始阶段,甲烷蒸汽重整的反应速率小于甲烷氧化的反应速率,故答案为:小于;
(3)根据平衡常数k的表达式,可知反应CH4(g)+H2O(g)?CO(g)+3H2(g)的KP=
| p3(H2)?P(CO) |
| P(CH4)?P(H2O) |
该反应为吸热反应,升高温度,平衡向正反应移动,平衡常数增大,
故答案为:
| p3(H2)?P(CO) |
| P(CH4)?P(H2O) |
(4)从能量的角度分析,甲烷自热重整方法的先进之处在于:放热的甲烷氧化反应为吸热的蒸气重整提供能量,提高能源的利用率,故答案为:放热的甲烷氧化反应为吸热的蒸气重整提供能量;
(5)①由图中数据可知,0.9 MPa时,H2的物质的量分数>65%,CO物质的量分数<10%,则700℃符合,1.5 MPa时,H2的物质的量分数>65%,CO物质的量分数<10%,则温度要高于750℃,低于约725℃,矛盾,故B正确,ACD错误,故答案为:B;
②起始进料时H2的物质的量分数为0,结合图象可知600℃,0.1 MPa的条件下,平衡时系统中H2的物质的量分数达到70%,据此画出H2的物质的量分数随时间变化的示意图为
 ,
,故答案为:
 ;
;(6)如果反应过程中进氧气的量过大,会导致生成的氢气和氧气反应,导致质量分数降低,
故答案为:导致生成的氢气和氧气反应.
点评:本题考查热化学以及化学反应速率、化学平衡等,意在考查考生分析、处理数据和解答图象试题的能力,解答本题需利用盖斯定律,联系化学平衡、化学平衡常数以及平衡移动原理等,弄清图象的含义.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
.[2012·浙江卷] 水溶液X中只可能溶有K+、Mg2+、Al3+、AlO2-、SiO32-、SO32-、CO32-、SO42-中的若干种离子。某同学对该溶液进行了如下实验: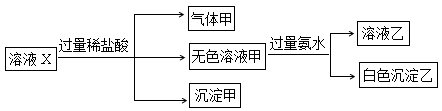
下列判断正确的是( )
| A.气体甲一定是纯净物 |
| B.沉淀甲是硅酸和硅酸镁的混合物 |
| C.K+、AlO2-和SiO32-一定存在于溶液X中 |
| D.CO32-和SO42-一定不存在于溶液X中 |

 (2012?浙江模拟)学校化学研究小组对某溶液进行检测分析,该无色溶液中可能含有NH4+、K+、Al3+、HCO3-、Cl-、MnO4-、SO42-等离子中的几种离子.
(2012?浙江模拟)学校化学研究小组对某溶液进行检测分析,该无色溶液中可能含有NH4+、K+、Al3+、HCO3-、Cl-、MnO4-、SO42-等离子中的几种离子.
