题目内容
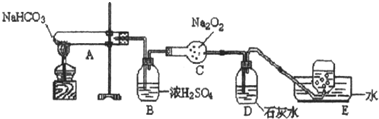
按以下装置图进行实验,填写有关现象及化学方程式

①A中现象是
②B中浓硫酸的作用是
③C中发生反应的化学方程式为
④D中现象是
⑤E中收集的气体是

①A中现象是
试管内壁有无色液滴
试管内壁有无色液滴
.②B中浓硫酸的作用是
干燥气体(吸收H2O)
干燥气体(吸收H2O)
.③C中发生反应的化学方程式为
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
.④D中现象是
石灰水变浑浊
石灰水变浑浊
,反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
.⑤E中收集的气体是
O2
O2
.分析:碳酸氢钠分解生成二氧化碳和水,浓硫酸具有吸水性,可用于干燥二氧化碳气体,在C中二氧化碳和过氧化钠反应生成碳酸钠和氧气,二氧化碳通入澄清石灰水中发生反应生成碳酸钙沉淀,氧气不溶于水,可用排水法收集.
①根据碳酸氢钠受热分解的产物进行回答;
②根据浓硫酸的性质分析;
③根据过氧化钠的性质分析;
④根据二氧化碳和石灰水的性质分析;
⑤根据反应后可能剩余的气体分析.
①根据碳酸氢钠受热分解的产物进行回答;
②根据浓硫酸的性质分析;
③根据过氧化钠的性质分析;
④根据二氧化碳和石灰水的性质分析;
⑤根据反应后可能剩余的气体分析.
解答:解:①碳酸氢钠受热分解生成碳酸钠、水以及二氧化碳,会看到试管内壁有无色液滴,故答案为试管内壁有无色液滴;
②浓硫酸有吸水性,所以能作干燥剂,二氧化碳和浓硫酸不反应,所以能用浓硫酸干燥二氧化碳,故答案为:干燥气体(吸收H2O);
③二氧化碳和过氧化钠反应生成碳酸钠和氧气2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2;
④二氧化碳能使澄清的石灰水变浑浊,所以未与过氧化钠反应的二氧化碳使石灰水变浑浊,发生反应的离子方程式为CO2+Ca2++2OH-=CaCO3↓+H2O,
故答案为:石灰水变浑浊;CO2+Ca2++2OH-=CaCO3↓+H2O;
⑤碳酸氢钠分解生成的水蒸汽被浓硫酸吸收,未与过氧化钠反应的二氧化碳被石灰水吸收,所以剩余的气体就是二氧化碳和过氧化钠反应生成的氧气,故答案为:O2.
②浓硫酸有吸水性,所以能作干燥剂,二氧化碳和浓硫酸不反应,所以能用浓硫酸干燥二氧化碳,故答案为:干燥气体(吸收H2O);
③二氧化碳和过氧化钠反应生成碳酸钠和氧气2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2;
④二氧化碳能使澄清的石灰水变浑浊,所以未与过氧化钠反应的二氧化碳使石灰水变浑浊,发生反应的离子方程式为CO2+Ca2++2OH-=CaCO3↓+H2O,
故答案为:石灰水变浑浊;CO2+Ca2++2OH-=CaCO3↓+H2O;
⑤碳酸氢钠分解生成的水蒸汽被浓硫酸吸收,未与过氧化钠反应的二氧化碳被石灰水吸收,所以剩余的气体就是二氧化碳和过氧化钠反应生成的氧气,故答案为:O2.
点评:本题考查了碳酸氢钠加热易分解的性质,书写过氧化钠与二氧化碳反应的化学方程式时,生成的氧气不能写气体符号;在离子方程式中,微溶物的澄清液写离子形式,浑浊或沉淀时写化学式.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目