题目内容
7g炭粉与14g氧气在一定条件下完全反应生成21g氧化物,则生成物中CO与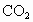 的物质的量之比为
的物质的量之比为
[ ]
|
A.1∶1 |
B.2∶1 |
C.2∶3 |
D.3∶1 |
答案:A
解析:
解析:
|
解法 1:碳与氧气反关应,有以下两种情况: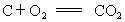 ; ;
 的物质的量为y.根据质量守恒定律,有: 的物质的量为y.根据质量守恒定律,有:
x+y=7g÷12g/mol ① (碳守恒);x+2y=14g÷16g/mol ② (氧守恒);联立①、②求解,得:x=7/24mol,y=7/24mol,x∶y=1∶1. 解法 2:对此题,由于题目所要求的是CO和 的物质的量之比,可先考虑求C与O的物质的量之比,(7g÷12g/mol)∶(14g÷16g/mol)=2∶3.假定C的物质的量为2mol,O的物质的量为3mol. 的物质的量之比,可先考虑求C与O的物质的量之比,(7g÷12g/mol)∶(14g÷16g/mol)=2∶3.假定C的物质的量为2mol,O的物质的量为3mol.
然后,设生成物中 CO的物质的量为x, 的物质量为y.根据质量守恒定律,有:x+y=2mol ①,x+2y=3mol ②,联立①、②求解,得:x∶y=1∶1. 的物质量为y.根据质量守恒定律,有:x+y=2mol ①,x+2y=3mol ②,联立①、②求解,得:x∶y=1∶1.
解法 3:分析仍同“解法1”,解题用“差量法”.CO中1molC对应1molO,而  中1molC对应1mol 中1molC对应1mol  显然,若1mol 显然,若1mol  取代1mol CO的位置,C的物质的量不变,O的物质的量增加1mol,即它们所对应的关系是1∶1的关系. 取代1mol CO的位置,C的物质的量不变,O的物质的量增加1mol,即它们所对应的关系是1∶1的关系.
根据前面分析,设混合气体中 C的物质的量为2mol,O的物质的量为3mol,其中 的物质的量为x有:1∶1=(3mol-2mol)∶x,x=1mol,n(CO)=2mol-1mol=1mol(守恒), 的物质的量为x有:1∶1=(3mol-2mol)∶x,x=1mol,n(CO)=2mol-1mol=1mol(守恒), .故答案选A. .故答案选A.
“守恒法”、“差量法”是高中化学计算中经常用到的“巧解方法”,它可以使化学计算变得更直观、更简单,从而提高学习效率和思维的敏捷性. |

练习册系列答案
相关题目
将7g炭粉与14g氧气在一定条件下完全反生成21g氧化物,则生成物中CO与CO2的物质的量之比为
| A.1:1 | B.2:1 | C.2:3 | D.3:1 |