题目内容
铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4?5H2O呈蓝色等.研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究.
Ⅰ.查阅资料:①Cu2O属于碱性氧化物; ②在空气中灼烧Cu2O生成CuO;③Cu2O在酸性条件下能发生下列反应:Cu2O+2H+═Cu+Cu2++H2O.
Ⅱ.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察溶液是否呈蓝色
(1)请你评价方案1和方案2.如果你认为方案合理,请简述其化学原理;如果你认为该方案不合理,请简述原因.
方案1: ;
方案2: .
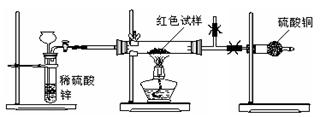
Ⅲ.研究性学习小组乙,设计了新的探究方案,拟通过干燥管中CuSO4是否变蓝判断红色固体中是否含有Cu2O,装置如图所示.
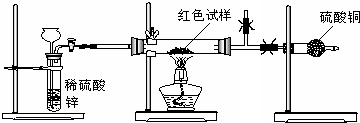
(2)为确保探究的科学、合理、安全,你认为实验中还应采取的措施有: (填序号)
A.在氢气发生器与硬质玻璃管之间加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管.
Ⅰ.查阅资料:①Cu2O属于碱性氧化物; ②在空气中灼烧Cu2O生成CuO;③Cu2O在酸性条件下能发生下列反应:Cu2O+2H+═Cu+Cu2++H2O.
Ⅱ.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察溶液是否呈蓝色
(1)请你评价方案1和方案2.如果你认为方案合理,请简述其化学原理;如果你认为该方案不合理,请简述原因.
方案1:
方案2:
Ⅲ.研究性学习小组乙,设计了新的探究方案,拟通过干燥管中CuSO4是否变蓝判断红色固体中是否含有Cu2O,装置如图所示.

(2)为确保探究的科学、合理、安全,你认为实验中还应采取的措施有:
A.在氢气发生器与硬质玻璃管之间加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管.
分析:(1)根据铜和氧化亚铜都能和硝酸生成Cu2+;Cu+在酸性条件下能发生自身氧化还原反应,也生成了铜单质,金属铜和稀硫酸不反应来回答;
(2)根据水的存在会对实验结果造成误差来回答判断.
(2)根据水的存在会对实验结果造成误差来回答判断.
解答:解:(1)因为硝酸具有酸性和氧化性,铜和氧化亚铜均可溶于稀硝酸形成硝酸铜蓝色溶液,金属铜的干扰导致无法判断所得红色固体中是否含有Cu2O,即方案1不合理,取该红色试样溶于足量的稀硫酸中,因为只有氧化亚铜与稀硫酸生成Cu和Cu2+,导致溶液呈蓝色,而铜不与稀硫酸发生反应,所以根据溶液是否变蓝确定是否含有氧化亚铜,即方案2合理,
故答案为:方案1不合理,因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液;方案2合理,因为氧化亚铜与稀硫酸生成Cu和Cu2+,导致溶液呈蓝色,而铜不与稀硫酸发生反应;
(2)根据硫酸铜是否变蓝判断是否含有氧化亚铜时,要注意水的干扰因素,所以制取的氢气要干燥,可以在氢气发生器与硬质玻璃管之间加一个干燥装置,并且要将空气中的水的干扰排除,可以在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管,实验前要将装置中的空气排净,防止干扰,
故答案为:ABC.
故答案为:方案1不合理,因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液;方案2合理,因为氧化亚铜与稀硫酸生成Cu和Cu2+,导致溶液呈蓝色,而铜不与稀硫酸发生反应;
(2)根据硫酸铜是否变蓝判断是否含有氧化亚铜时,要注意水的干扰因素,所以制取的氢气要干燥,可以在氢气发生器与硬质玻璃管之间加一个干燥装置,并且要将空气中的水的干扰排除,可以在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管,实验前要将装置中的空气排净,防止干扰,
故答案为:ABC.
点评:本题是一道性质实验方案的设计考题,注意知识的迁移和应用是解题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目