题目内容
(6分) 铅蓄电池是最普通的二次电源,其电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O。已知PbSO4是难溶性的电解质,根据上述情况判断:
(1)蓄电池的负极是 ,其电极反应方程式为 。
(2)蓄电池的正极反应方程式为:PbO2 + 2e- + 4H+ +SO42- = PbSO4 + 2H2O,当电路中转移3mol电子时,被还原的PbO2的物质的量为 。
(3)蓄电池工作时,其中电解质溶液的pH______(填“增大”、“减小”、“不变”)。
(1)蓄电池的负极是 ,其电极反应方程式为 。
(2)蓄电池的正极反应方程式为:PbO2 + 2e- + 4H+ +SO42- = PbSO4 + 2H2O,当电路中转移3mol电子时,被还原的PbO2的物质的量为 。
(3)蓄电池工作时,其中电解质溶液的pH______(填“增大”、“减小”、“不变”)。
(6分)(1)Pb ;Pb-2e- + SO42- =" " PbSO4 (2)1.5mol (3)增大
略

练习册系列答案
相关题目
 Cd+2NiO(OH)+2H2O 则,该电池放电时的负极材料是( )。
Cd+2NiO(OH)+2H2O 则,该电池放电时的负极材料是( )。 作原理如右图所示。
作原理如右图所示。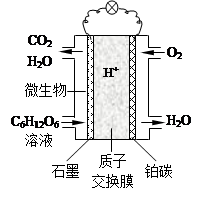
 已知石墨电极上反应为:
已知石墨电极上反应为: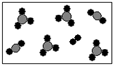
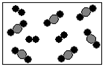
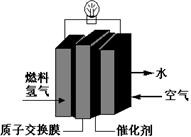
 2PbSO4 + 2H2O,则下列说法正确的是
2PbSO4 + 2H2O,则下列说法正确的是