题目内容
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:
MgSO4(s)+CO(g)?MgO(s)+CO2(g)+SO2(g)△H>0
该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
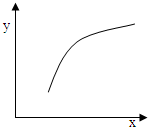
MgSO4(s)+CO(g)?MgO(s)+CO2(g)+SO2(g)△H>0
该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
| 选项 | x | y |
| A | 温度 | 容器内混合气体的密度 |
| B | CO的物质的量 | CO2与CO的物质的量之比 |
| C | SO2的浓度 | 平衡常数K |
| D | MgSO4的质量(忽略体积) | CO的转化率 |
| A.A | B.B | C.C | D.D |

该反应为正方向体积增加且吸热.
A、升高温度,平衡正向移动,气体的质量增加,密度增大,故A正确;
B、增加CO的量,平衡正向移动,但压强增大,转化的量,没有上一平衡多,故比值减小,故B错误;
C、平衡常数只与温度有关,浓度变化平衡常数不变,故C错误;
D、因MgSO4为固体,增加其量,对CO的转化率无影响,故D错误;
故选A.
A、升高温度,平衡正向移动,气体的质量增加,密度增大,故A正确;
B、增加CO的量,平衡正向移动,但压强增大,转化的量,没有上一平衡多,故比值减小,故B错误;
C、平衡常数只与温度有关,浓度变化平衡常数不变,故C错误;
D、因MgSO4为固体,增加其量,对CO的转化率无影响,故D错误;
故选A.

练习册系列答案
 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案
相关题目