题目内容
燃烧a g乙醇(液),生成二氧化碳气体和液态水,放出的热量为QKJ,经测定,a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L(氢气中H原子为羟基上H原子),则乙醇燃烧的热化学方程式书写正确的是( )A.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-QkJ/mol
B.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-Q/2kJ/mol
C.
 C2H5OH(1)+
C2H5OH(1)+ O2(g)=CO2(g)+
O2(g)=CO2(g)+ H2O(1)△H=-QkJ/mol
H2O(1)△H=-QkJ/molD.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-2QkJ/mol
【答案】分析:由a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L,可知a g乙醇的物质的量为0.5mol.由于燃烧a g乙醇(液),生成二氧化碳气体和液态水,放出的热量为QKJ,即燃烧0.5mol乙醇(液),生成二氧化碳气体和液态水,放出的热量为QKJ.据此写出热化学反应方程式,进行判断.
解答:解:a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L,
则生成氢气的物质的量为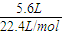 =0.25mol.
=0.25mol.
由2C2H5OH~H2可知,a g乙醇的物质的量为0.5mol.
由于燃烧a g乙醇(液),生成二氧化碳气体和液态水,放出的热量为QKJ,
燃烧0.5mol乙醇(液),生成二氧化碳气体和液态水,放出的热量为QKJ.
该条件下乙醇燃烧的热化学方程式为: C2H5OH(1)+
C2H5OH(1)+ O2(g)=CO2(g)+
O2(g)=CO2(g)+ H2O(1)△H=-QkJ/mol
H2O(1)△H=-QkJ/mol
或C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-2QkJ/mol.
故选:CD.
点评:考查热化学反应方程式的书写,难度不大,关键根据氢气的体积计算出乙醇的物质的量.
解答:解:a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L,
则生成氢气的物质的量为
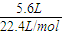 =0.25mol.
=0.25mol.由2C2H5OH~H2可知,a g乙醇的物质的量为0.5mol.
由于燃烧a g乙醇(液),生成二氧化碳气体和液态水,放出的热量为QKJ,
燃烧0.5mol乙醇(液),生成二氧化碳气体和液态水,放出的热量为QKJ.
该条件下乙醇燃烧的热化学方程式为:
 C2H5OH(1)+
C2H5OH(1)+ O2(g)=CO2(g)+
O2(g)=CO2(g)+ H2O(1)△H=-QkJ/mol
H2O(1)△H=-QkJ/mol或C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-2QkJ/mol.
故选:CD.
点评:考查热化学反应方程式的书写,难度不大,关键根据氢气的体积计算出乙醇的物质的量.

练习册系列答案
相关题目