题目内容
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过。下列有关叙述不正确的是
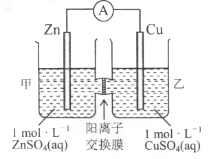
A. 锌电极上发生氧化反应
B. 电池工作一段时间后,甲池的c(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阳离子通过交换膜向正极移动,保持溶液中电荷平衡
【答案】B
【解析】
在上述原电池中,锌电极为负极,锌原子失去电子被氧化成锌离子。电子沿着外接导线转移到铜电极。铜电极为正极,溶液中的铜离子在铜电极上得到电子被还原成铜单质。电解质溶液中的阳离子向正极移动,而阴离子向负极移动。
A. 铜电极为正极,锌电极为负极,负极发生氧化反应,A项正确;
B. 电解质溶液中的阳离子向正极移动,而阴离子向负极移动。但是阳离子交换膜只允许阳离子和水分子通过,SO42-不能通过阳离子交换膜,并且甲池中硫酸根不参加反应,因此甲池的c(SO42-)不变,B项错误;
C. 锌原电池,锌作负极,铜作正极,铜离子在铜电极上沉淀,锌离子通过阳离子交换膜进入乙池,每沉淀1mol,即64g铜,就补充过来1mol锌离子,其质量为65g,所以工作一段时间后乙池溶液的质量不断增加,C项正确;
D. 原电池中,阳离子通过阳离子交换膜向正极移动,使溶液保持电中性,维持电荷平衡,D项正确;
答案选B。

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目