题目内容
有A、B、C三种不溶于水的透明晶体,A在氧气中燃烧时可生成一种无色无臭的气体D,且D的密度为同温同压下氢气密度的22倍;B与苛性钠溶液反应可生成盐E,E的水溶液中通入D的气体可析出白色胶状沉淀,此沉淀溶于苛性钠溶液也可得到盐E;C是B与石灰石、纯碱按一定比率熔合成的无固定熔点的物质。
(1)推断A~E物质
A的名称______________,B的名称______________,C的名称______________,D的化学式______________,E的化学式______________。
(2)写离子方程式:
B→E:_______________________________________________________________
E+CO2:_______________________________________________________________
(3)B![]() C的化学方程式:_______________________,_____________________。
C的化学方程式:_______________________,_____________________。
(1)金刚石、水晶、玻璃,CO2,Na2SiO3 (2)SiO2+2OH-=SiO32-+H2O SiO32-+CO2+H2O=H2SiO3+CO32- (3)SiO2+CaCO3![]() CaSiO3+CO2↑ SiO2+Na2CO3
CaSiO3+CO2↑ SiO2+Na2CO3![]() Na2SiO3+CO2↑
Na2SiO3+CO2↑

练习册系列答案
相关题目
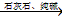 C的化学方程式:_______________________,_____________________。
C的化学方程式:_______________________,_____________________。