题目内容
如图所示“合成氨”的演示实验(夹持仪器均已省略)。在Y形管的一侧用Zn粒和稀H2SO4反应制取H2,另一侧用NaNO2固体和NH4Cl饱和溶液反应制取N2,N2和H2混合后通过还原铁粉来合成NH3,再将产生的气体通入酚酞试液中,若酚酞试液变红,则说明产生了氨气。

某课外活动小组通过查阅资料和多次实验,得到了如下信息:
信息一:NaNO2固体和饱和NH4Cl溶液混合加热的过程中发生如下反应:
①NaNO2+NH4Cl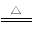 NH4NO2+NaCl
NH4NO2+NaCl
②NH4NO2 NH3↑+HNO2
NH3↑+HNO2
③2HNO2 N2O3↑+H2O
N2O3↑+H2O
④2NH3+N2O3 2N2+3H2O
2N2+3H2O
信息二:查阅资料,不同体积比的N2、H2混合气体在相同实验条件下合成氨,使酚酞试液变红所需要的时间如下:
N2和H2的体积比 | 5∶1 | 3∶1 | 1∶1 | 1∶3 | 1∶5 |
酚酞变红色所需时间/min | 8~9 | 7~8 | 6~7 | 3~4 | 9~10 |
据此回答下列问题:
(1)Y形管左侧管中发生反应的离子方程式________________________。
(2)铁粉撒在石棉绒上的目的是_________________________________
(3)课外活动小组的同学们认为,该实验中即使酚酞变红也不能说明N2和H2反应合成了NH3,得出此结论的理由是________________________。
请你另设计一个简单的实验验证你的理由____________________。欲解决这一问题,可以选用下图中的________装置连接在原装置中的________和________之间。
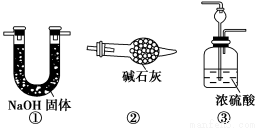
(4)在上述实验过程中,为尽快观察到酚酞试液变红的实验现象,应该控制N2和H2的体积比为________比较适宜;但该装置还难以实现此目的,原因是______________________________________。
(5)实验过程中通入试管C中的气体成分有________。
(1)Zn+2H+=Zn2++H2↑
(2)增大混合气体与催化剂的接触面积,使反应进行得更快
(3)从分步反应可知,产生N2的过程中,有可能直接产生氨气 将混合加热产生的气体直接通入酚酞试液,若试液变红,则说明理由成立;否则,说明理由不成立 ③ A B
(4)1∶3 无法控制通入B中N2和H2的体积比
(5)NH3、N2、H2
【解析】(1)根据Y形管右侧管需加热,说明右侧管反应制取N2,左侧管反应制取H2。(2)铁粉撒在石棉绒上的目的是增大与混合气体的接触面积,从而提高催化效率,增大反应速率。(3)因为NH4NO2分解可产生NH3,所以不能证明N2和H2反应生成了NH3。直接将Y形管中混合气体通入酚酞试液,若试液变红,则理由成立,否则理由不成立。在A、B之间加一个除NH3的装置,排除了NH3的干扰。(4)由表可知V(N2)∶V(H2)=1∶3时,反应最快,在Y形管中,无法控制气体的体积。(5)气体成分中有生成的NH3,同时还有未反应的N2、H2。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案