题目内容
如图表示金属X、Y及它们的合金Z分别与足量盐酸反应放出H2量的情况,横坐标表示消耗金属的物质的量,纵坐标表示在标准状况下产生H2的体积.下列有关合金组成的判断正确的是
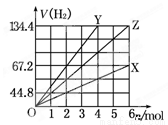
A.n(Na)∶n(Fe)=2∶1 B.n(Mg)∶n(K)=1∶2
C.n(Na)∶n(Al)=1∶3 D.n(K)∶n(Al)=1∶1
练习册系列答案
相关题目
硫酸铜的制备实验是无机化学实验教学中一个必做实验,某研究性学习小组设计了如下两个实验方案:
实验一:
因铜不能与稀硫酸反应,实验中用铜和浓硫酸加热使之完全反应,将溶液通过蒸发、结晶等操作得到硫酸铜晶体。
(1)浓硫酸与稀硫酸相比较,浓硫酸具有 。
(2)该反应的化学方程式为 。
实验二:
以空气为氧化剂的一步氧化法,将空气或氧气直接通入到铜粉与稀硫酸的混合物中,反应原理为2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ,但反应速率太慢,当升高温度到80~90℃,反应仍然缓慢。如在铜粉和稀硫酸的混合物中加入少量Fe2(SO4)3溶液,则速率明显加快。
(3)Fe2(SO4)3的作用是_________________。
(4)得到的混合液可以用下列四种物质中的_______调节pH =2~4,使Fe3+ 形成Fe(OH)3沉淀而除去:
A.NaOH B.CuO C.CuCO3 D.Fe
(5)请根据以上内容,对这两个实验方案进行评价,填下表:(至少写一点)
实 验 (一) | 实 验 (二) | |
主要优 点 | 操作简便 | (1)原料充分转化为产品 (2)没有有害气体排放 |
主要缺 点 |


 焰色为紫色,则原溶液的溶质一定就是钾盐
焰色为紫色,则原溶液的溶质一定就是钾盐 定时,滴定管尖端处有气泡,滴定完毕排出气泡。
定时,滴定管尖端处有气泡,滴定完毕排出气泡。 中”),其原因是:____________(用离子方程式表示)。
中”),其原因是:____________(用离子方程式表示)。 ol·L-1
ol·L-1 eC(g)+ fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是
eC(g)+ fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是