题目内容
【题目】乙烯是一种重要的化工原料,我们已学过用两种方法制得乙烯: 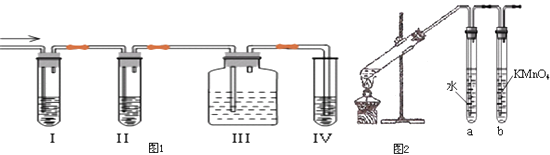
A.在实验室里用乙醇与浓硫酸共热制乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计如图1以确认上述混合气体中有C2H4和SO2 . 回答下列问题:
(1)I、II、III、IV装置中,可盛放的试剂顺序是(将下列有关试剂的序号填入空格内).
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是 .
(3)确定含有乙烯的现象是 .
(4)写出生成乙烯的反应方程式: .
B.为检验利用溴乙烷发生消去反应后生成的气体中是否含乙烯的装置如图2所示.回答:
①利用溴乙烷发生消去反应的化学方程式为:;
②试管a的作用是;若省去试管a,试管b中试剂为 .
【答案】
(1)A;B;A;D
(2)Ⅰ中品红溶液褪色
(3)Ⅲ中的品红不褪色,Ⅳ中的酸性高锰酸钾溶液褪色
(4)CH3CH2OH ![]() CH2=CH2↑+H2O;CH3CH2Br+NaOH
CH2=CH2↑+H2O;CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O;除去挥发出来的乙醇;溴水或溴的四氯化碳溶液
CH2=CH2↑+NaBr+H2O;除去挥发出来的乙醇;溴水或溴的四氯化碳溶液
【解析】解:A.(1)检验二氧化硫用品红溶液,检验乙烯用高锰酸钾酸性溶液,乙烯和二氧化硫都能使高锰酸钾酸性溶液褪色,所以先检验二氧化硫,然后检验乙烯,同在检验乙烯之前用NaOH溶液除尽SO2 , 再通过品红溶液不褪色确认SO2已除干净,最后用高锰酸钾酸性溶液褪色检验乙烯,因装置I用来检验SO2 , 试管中品红溶液褪色,说明含有SO2 , 装置II试管装有NaOH溶液除去SO2 , 装置III试管通过品红溶液不褪色确认SO2已除干净,装置IV 通过高锰酸钾酸性溶液褪色检验乙烯,所以答案是:A;B;A;D;
(2.)装置I用来检验SO2 , 试管中品红溶液褪色,说明含有SO2 , 所以答案是:Ⅰ中品红溶液褪色;
(3.)装置Ⅳ通过高锰酸钾酸性溶液褪色检验乙烯,如果Ⅲ中的品红不褪色,Ⅳ中的酸性高锰酸钾溶液褪色,则证明有乙烯生成,所以答案是:Ⅲ中的品红不褪色,Ⅳ中的酸性高锰酸钾溶液褪色;
(4.)乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应的化学方程式为:CH3CH2OH ![]() CH2=CH2↑+H2O,所以答案是:CH3CH2OH
CH2=CH2↑+H2O,所以答案是:CH3CH2OH ![]() CH2=CH2↑+H2O; B.
CH2=CH2↑+H2O; B.
①溴乙烷从一个分子中脱去一个溴化氢分子,溴乙烷中的碳碳单键变为双键,反应的方程式为:CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O,
CH2=CH2↑+NaBr+H2O,
所以答案是:CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O;
CH2=CH2↑+NaBr+H2O;
②乙醇沸点低,易挥发,但乙醇与水可以任意比互溶;乙烯和溴水中的溴发生加成反应,溴水褪色,乙醇与溴水不反应,可检验乙烯的存在;所以答案是:除去挥发出来的乙醇;溴水或溴的四氯化碳溶液.

 阅读快车系列答案
阅读快车系列答案