题目内容
3. 25℃时,将浓度均为0.lmol/lHX溶液和HY溶液分别与等浓度的NaHCO3溶液DENG 体积混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示:下列说法正确的是( )
25℃时,将浓度均为0.lmol/lHX溶液和HY溶液分别与等浓度的NaHCO3溶液DENG 体积混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示:下列说法正确的是( )| A. | 相同浓度的HX和HY溶液中水的电离程度:HX<HY | |
| B. | 相同体积相同浓度的NaX和NaY溶液中阴离子数目前者大于后者 | |
| C. | 向10mL0.1mol/L的Na2CO3溶液中缓慢滴加10mol/L的HY,混合后的离子浓度大小关系:c(Na+)>c (Y-)>c (HCO3-)>c (H+) | |
| D. | 将等体积等浓度的HX和HY溶液分别用相同的氢氧化钠溶液滴定,至中性时,消耗的氢氧化钠溶液体积前者大于后者 |
分析 HY与NaHCO3溶液反应速率快,溶液中氢离子浓度大,所以HY的酸性大于HX,则酸性的比较:HY>HX>H2CO3,
A.浓度相同的HX和HY溶液中氢离子浓度HY大于HX,对水电离抑制程度HY抑制程度大;
B.酸性的比较:HY>HX,则NaX和NaY溶液水解程度NaX>NaY,电荷守恒分析判断阴离子数目大小;
C.酸性的比较:HY>HX>H2CO3,向10mL 0.1mol/L的Na2CO3溶液中缓慢滴加10mL0.1mol/L的HY,反应生成碳酸氢钠溶液和NaY溶液的混合物,Y-离子水解程度小于HCO3-,据此判断离子浓度大小;
D.将等体积等浓度的HX和HY溶液分别用相同浓度的氢氧化钠溶液滴定,酸性的比较:HY>HX,至中性时HX消耗的氢氧化钠溶液体积小.
解答 解:A.酸性的比较:HY>HX,浓度相同的HX和HY溶液中氢离子浓度HY大于HX,对水电离抑制程度HY抑制程度大,相同浓度的HX和HY溶液中水的电离程度:HX>HY,故A错误;
B.溶液中电荷守恒,c(Na+)+c(H+)=c(X-)+c(OH-),c(Na+)+c(H+)=c(Y-)+c(OH-),c(Na+)浓度相同,酸性的比较:HY>HX,则NaX和NaY溶液水解程度NaX>NaY,NaX溶液中氢氧根离子浓度大于NaY溶液中氢氧根离子浓度,则NaX溶液中氢离子浓度小于NaY溶液中氢离子浓度,相同体积相同浓度的NaX和NaY溶液中阴离子数目NaY大于NaX,故B错误;
C.酸性的比较:HX>HY>H2CO3,向10mL 0.1mol/L的Na2CO3溶液中缓慢滴加10mL0.1mol/L的HY,反应生成碳酸氢钠溶液和NaY溶液的混合物,Y-离子水解程度小于HCO3-,据此判断离子浓度大小c (Na+)>c (Y-)>c (HCO3-)>c (H+),故C正确;
D.将等体积等浓度的HX和HY溶液分别用相同浓度的氢氧化钠溶液滴定,酸性的比较:HY>HX,则NaX溶液碱性大于NaY溶液,反应至中性时HX消耗的氢氧化钠溶液体积小,故D错误;
故选C.
点评 本题考查了弱电解质电离平衡影响因素、盐类水解程度大小比较、离子浓度大小比较、电解质溶液中电荷守恒等知识点,掌握基础是解题关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | H+、OH-、Na+、SO42- | B. | Fe2+、OH-、K+、C1- | ||
| C. | Cu2+、NO3-、C1-、Na+ | D. | Ba2+、C1-、CO32-、Na+ |
| A. | 明矾易溶于水,可用作净水剂 | |
| B. | 浓硫酸具有脱水性,可用于干燥氢气 | |
| C. | 二氧化锰具有催化作用,可用于实验室制氯气 | |
| D. | 液氨汽化时要吸收大量的热,可用作制冷剂 |
| A. | 乙烷中是否混有乙烯,可通过溴水观察是否褪色进行检验 | |
| B. | 乙醇中是否混有水,可加无水硫酸铜粉末观察是否变蓝进行检验 | |
| C. | 乙醇中是否混有乙酸,可加入金属钠观察是否产生气体进行检验 | |
| D. | 乙酸乙酯中是否混有乙酸,可加石蕊试液观察是否变红进行检测 |
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A. | 反应 CN-+H2O+CO2═HCN+HCO3-能够发生 | |
| B. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量,前者小于后者 | |
| C. | 物质的量浓度相等的 HCOONa 和 KCN 溶液中:c(Na+)-c(HCOO-)<c(K+)-c(CN-) | |
| D. | c(NH4+)相等的 HCOONH4 溶液、NH4CN 溶液、NH4HCO3 溶液:c(NH4HCO3)>c(NH4CN)>c(HCOONH4) |
 ④
④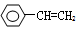 ⑤
⑤ 既能使酸性高锰酸钾溶液褪色,又能使溴水反应褪色的是( )
既能使酸性高锰酸钾溶液褪色,又能使溴水反应褪色的是( )| A. | ①④ | B. | ②③ | C. | ②⑤ | D. | ③⑤ |
| A. | 2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑ | |
| B. | NaOH+HCl═NaCl+H2O | |
| C. | CaO+H2O═Ca(OH)2 | |
| D. | NH4Cl$\frac{\underline{\;加热\;}}{\;}$NH3↑+HCl↑ |
| A. | 尼龙绳主要由合成纤维制造 | |
| B. | 烷烃沸点随分子中碳原子数的增加,逐渐升高 | |
| C. | 乙烷是一种植物生长调节剂,可用作水果的催熟剂 | |
| D. | 化合物  、 、 、 、 的分子式均为C6H6,它们互为同分异构体 的分子式均为C6H6,它们互为同分异构体 |
 、HCHO、CH3COCH3、HCOOH、HCOOCH3.
、HCHO、CH3COCH3、HCOOH、HCOOCH3.