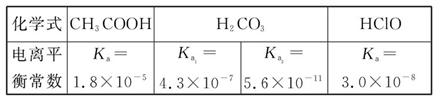
题目内容
0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是( )
①电离程度增大;②c(NH3·H2O)增大;③NH4+数目增多;④c(OH-)增大;⑤导电性增强;⑥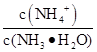 增大
增大
①电离程度增大;②c(NH3·H2O)增大;③NH4+数目增多;④c(OH-)增大;⑤导电性增强;⑥
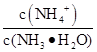 增大
增大| A.①②③ | B.①③⑤ | C.①③⑥ | D.②④⑥ |
C
NH3·H2O作为弱电解质加水稀释,电离程度增大,c(NH3·H2O)减小,NH4+和OH-的数目增多,但c(OH-)、c(NH4+)减小;导致溶液的导电性减弱;由于加水稀释,电离平衡向右移动,故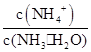 增大。
增大。
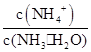 增大。
增大。
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
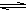 CH3COO- + H3O+
CH3COO- + H3O+