题目内容
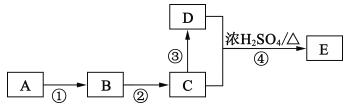
【题目】某研究小组以苯酚为主要原料,按下列路线合成药物——沙丁胺醇。
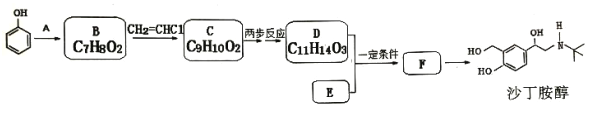
已知::①A→B 原子利用率为 100%
②R-OH![]() R-O-CH3; R-O-CH3
R-O-CH3; R-O-CH3 ![]() R-OH
R-OH
③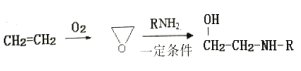
请回答:
(1)写出 C 中官能团的名称______________________________。
(2)B→C 反应类型为___________________________________。
(3)下列有关说法正确是_________。
A.A 是甲醛 B.苯酚有毒,但能用于杀菌消毒
C.化合物 D 与 FeCl3溶液发生显色反应 D.沙丁胺醇分子式: C13H21NO3
(4)设计化合物 C 经两步反应转变为 D 的合成路线(用流程图表示) _______________________________________________________________。
(5)写出 E 的结构简式_________________________________________。
(6)写出 F→ 沙丁胺醇反应的另一种反应物是_________________________。
(7)化合物 M 是 C 的同分异构体,M 符合下列条件的同分异构体有______种;
① M 苯环上只有两个对位取代基; ② 能发生水解反应;
写出其中 1H-NMR 谱中有 4 种氢原子的 M 所有可能的结构简式________________。
【答案】 羟基和碳碳双键 取代反应 ) ABD 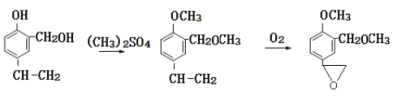
![]() HI 4 CH3(C6H4)COOCH3 或 CH3COO(C6H4)CH3(对位)
HI 4 CH3(C6H4)COOCH3 或 CH3COO(C6H4)CH3(对位)
【解析】A→B原子利用率为100%,A的分子式为CH2O,B与氯乙烯发生取代反应生成C,结合沙丁胺醇的结构简式B是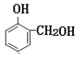 ,C是
,C是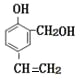 ,C中碳碳双键被氧化强需要保护羟基不被氧化,所以C→D的两步反应,
,C中碳碳双键被氧化强需要保护羟基不被氧化,所以C→D的两步反应, 先与(CH3)2SO4反应生成
先与(CH3)2SO4反应生成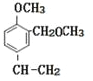 ,
, 再氧化为
再氧化为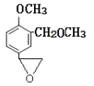 ,所以D为
,所以D为 ,结合沙丁胺醇的结构简式逆推E,E是
,结合沙丁胺醇的结构简式逆推E,E是![]() ,F为:
,F为: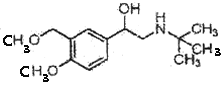 ,F与HI反应生成
,F与HI反应生成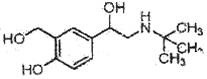 。(1)C为
。(1)C为 官能团的名称为羟基和碳碳双键;(2)B与氯乙烯发生取代反应生成C,
官能团的名称为羟基和碳碳双键;(2)B与氯乙烯发生取代反应生成C, →;(3)A.分析可知A是甲醛 CH2O,故A正确;B.苯酚有毒,但一定浓度的苯酚稀溶液能用于杀菌消毒,故B正确;C.化合物D为
→;(3)A.分析可知A是甲醛 CH2O,故A正确;B.苯酚有毒,但一定浓度的苯酚稀溶液能用于杀菌消毒,故B正确;C.化合物D为 ,分子中无酚羟基,与FeCl3溶液不发生显色反应,故C错误;D.沙丁胺醇结构简式为:
,分子中无酚羟基,与FeCl3溶液不发生显色反应,故C错误;D.沙丁胺醇结构简式为: ,分子式:C13H21NO3,故D正确;故选ABD;(4)C中碳碳双键被氧化强需要保护羟基不被氧化,所以C→D的两步反应,
,分子式:C13H21NO3,故D正确;故选ABD;(4)C中碳碳双键被氧化强需要保护羟基不被氧化,所以C→D的两步反应, 先与(CH3)2SO4反应生成
先与(CH3)2SO4反应生成 ,
, 再氧化为
再氧化为 ,所以D为
,所以D为 ,化合物
,化合物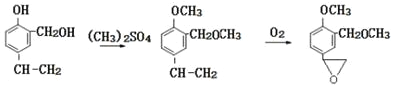 ;(5)E的结构简式为
;(5)E的结构简式为![]() ;(6)F为:
;(6)F为: ,F与HI反应生成
,F与HI反应生成 ,F→沙丁胺醇反应的另一种反应物是HI;(7)化合物M是C
,F→沙丁胺醇反应的另一种反应物是HI;(7)化合物M是C 的同分异构体,满足①M苯环上只有两个对位取代基;②能发生水解反应,一个取代基中含酯基结构分别为:CH3(C6H4)COOCH3、CH3COO(C6H4)CH3、CH3CH2(C6H4)OOCH、CH3(C6H4)CH2OOCH,其中1H-NMR谱中有4种氢原子的M所有可能的结构简式为:CH3(C6H4)COOCH3 或 CH3COO(C6H4)CH3(对位)。
的同分异构体,满足①M苯环上只有两个对位取代基;②能发生水解反应,一个取代基中含酯基结构分别为:CH3(C6H4)COOCH3、CH3COO(C6H4)CH3、CH3CH2(C6H4)OOCH、CH3(C6H4)CH2OOCH,其中1H-NMR谱中有4种氢原子的M所有可能的结构简式为:CH3(C6H4)COOCH3 或 CH3COO(C6H4)CH3(对位)。

 口算题天天练系列答案
口算题天天练系列答案【题目】某工厂酸性废液中含有Fe3+、Al3+、Fe2+、SO42-,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略):
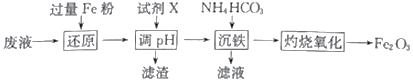
已知:①NH4HCO3在热水中会分解。
②常温下,溶液中不同金属离子生成氢氧化物沉淀时的pH见下表:
金属离子(0.1mol·L-l) | Fe3+ | Fe2+ | Al3+ |
开始沉淀时的pH | 2.4 | 7.6 | 3.4 |
完全沉淀时的pH | 3.7 | 9.6 | 4.8 |
回答下列问题:
(1)写出“还原”步骤中反应的离子方程式:_________________________________。
(2)试剂X可选用_________(任写一种,填化学式),“滤渣”的主要成分是_________________。
(3)加入碳酸氢铵后过滤,发现滤液仍然浑浊,可能的原因是_________________________,用90℃热水洗涤FeCO3沉淀的目的是______________________________________。
(4)若在实验室中灼烧FeCO3应在_____________(填仪器名称)中进行,“灼烧氧化”发生的化学方程式为__________________________________。
(5)若工业上灼烧氧化174.0吨FeCO3得到117.6吨产品,则该产品中Fe2O3的纯度为___________ (设产品中杂质只有FeO,保留一位小数)。
【题目】 Fe和Mg与H2SO4反应的实验如下:
实验 |
|
|
|
|
现象 | Fe表面产生大量无色气泡 | Fe表面产生气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是( )
A.I中产生气体的原因是:Fe + 2H+=Fe2++ H2↑
B.取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C.Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D.Ⅳ中现象说明Mg的金属性比Fe强