题目内容
某元素的最高价氧化物为R2O5,该元素的气态氢化物中氢的质量分数为8.82%,已知该元素原子核内中子数比核外电子数多1。试推断:
(1)该元素的名称是__________,在元素周期表中的位置是__________。
(2)该元素的最高价氧化物对应水化物的酸性强弱与同周期元素最高价含氧酸的比较应为(写出化学式)__________。
(1)磷 第3周期第ⅤA族
(2)HClO4>H2SO4>H3PO4>H2SiO3
解析:
最高价氧化物为R2O5,可知该元素气态氢化物为RH3。由质量分数计算:![]() ×100%=8.82%,Mr=31。所以该元素原子的质子数为
×100%=8.82%,Mr=31。所以该元素原子的质子数为![]() =15,为磷元素。
=15,为磷元素。

练习册系列答案
相关题目
(12分)下表为元素周期表的一部分,按要求完成各小题。
|
|
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
|
|
|
⑥ |
|
⑦ |
⑾ |
|
|
3 |
① |
③ |
⑤ |
|
|
|
⑧ |
⑩ |
|
4 |
② |
④ |
|
|
|
|
⑨ |
|
1.化学性质最不活泼的元素 (填元编号,下同),非金属性最强的元素是 金属性最强的单质与水反应的离子方程式为
2.①③⑤三种元素的最高价氧化物水化物中,碱性最强的
3.①③⑤三种元素的原子半径由大到小的顺序为
4.某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素为 在两种盐中该元素的化合价为 ,该元素的最高价氧化物和盐酸反应的化学方程式为 向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH至过量,现象为
 H2CO3+OH-
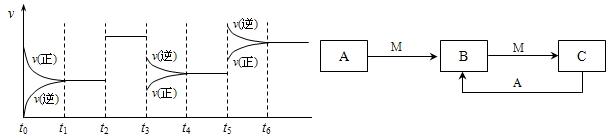
H2CO3+OH- 2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是
2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是 物质A、B、C有如图1转化关系:
物质A、B、C有如图1转化关系:
