题目内容
【题目】铜和浓硫酸发生反应的化学方程式为:Cu +2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_______剂,具有 性。在该反应中,若消耗了32gCu,则转移了_______mol 电子 ,生成 L SO2(标准状况)气体。
CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_______剂,具有 性。在该反应中,若消耗了32gCu,则转移了_______mol 电子 ,生成 L SO2(标准状况)气体。
【答案】
还原;还原;氧化;氧化;1;11.2;
【解析】
试题分析:反应Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O中,S元素化合价降低,被还原,发生还原反应,浓H2SO4作氧化剂,表现为氧化性,在该反应中,若消耗了32gCu,即0.5mol,则转移了1mol电子,生成0.5molSO2,标准条件下体积为11.2L,故答案为:还原;还原;氧化;氧化;1;11.2。
CuSO4+SO2↑+2H2O中,S元素化合价降低,被还原,发生还原反应,浓H2SO4作氧化剂,表现为氧化性,在该反应中,若消耗了32gCu,即0.5mol,则转移了1mol电子,生成0.5molSO2,标准条件下体积为11.2L,故答案为:还原;还原;氧化;氧化;1;11.2。

练习册系列答案
相关题目
【题目】利用如图所示装置分别盛放相应物质进行下列实验,得出结论正确的是
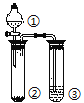
选项 | ① | ② | ③ | 判定结论 |
A | 浓硫酸 | 蔗糖 | 溴水 | 用来判定浓硫酸具有脱水性、氧化性 |
B | 稀盐酸 | Na2SO3 | Ba(NO3)2 | 用来判定SO2与可溶性钡盐均可生成白色沉淀 |
C | 浓盐酸 | Na2CO3 | Na2SiO3 | 用来判定酸性:盐酸>碳酸>硅酸 |
D | 浓硫酸 | Cu | NaOH | 用来判定制备SO2并吸收尾气 |
A. A B. B C. C D. D