题目内容
在0℃和101 kPa的条件下,将4.00 g 氩气、1.40 g 氮气和1.60 g 氧气混合,该混合气体的密度是相同条件下氢气密度的( )
A.35倍 B.17.5倍 C.7倍 D.14倍
【答案】
B
【解析】三种气体的物质的量分别是0.1mol、0.05mol和0.05mol,则混合气的平均相对分子质量是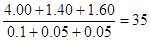 。由于在等温等压时,气体的密度之比是相应的摩尔质量之比,因此混合气的密度是相同条件下氢气密度的35÷17.5倍,答案选B。
。由于在等温等压时,气体的密度之比是相应的摩尔质量之比,因此混合气的密度是相同条件下氢气密度的35÷17.5倍,答案选B。

练习册系列答案
相关题目
|
在0℃和101 kPa的条件下,将2.00 g氦气、1.40 g氮气和1.60 g氧气混合,该混合气体的体积是 | |
| [ ] | |
A. |
6.72 L |
B. |
7.84 L |
C. |
10.08 L |
D. |
13.44 L |
在0℃和101 kPa的条件下,将4.00 g氩气、1.40 g氮气和1.60 g氧气混合,该混合气体的密度是相同条件下氢气密度的( )
| A.35倍 | B.17.5倍 | C.7倍 | D.14倍 |
在0℃和101 kPa的条件下,将4.00 g Ar、1.40 g N2和 1.60 g O2混合,该混合气体的体积是的密度是相同条件下氢气密度的
| A.35倍 | B.17.5倍 | C.7倍 | D.14倍 |