题目内容
下列表示对应化学反应的离子方程式正确的是
| A.过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| B.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O |
C.大理石溶于醋酸中的反应:CaCO3+2H+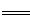 Ca2++H2O+CO2↑ Ca2++H2O+CO2↑ |
D.等物质的量的NaHCO3和Ca(OH)2溶液混合:2 HCO3-+Ca2++2OH- CaCO3↓+ CO32-+2H2O CaCO3↓+ CO32-+2H2O |
B
解析试题分析:过量石灰水与碳酸氢钙反应,碳酸氢根少,钙离子过量,碳酸氢根前系数应该为1,正确的离子方程式是Ca2++HCO3-+OH-=CaCO3↓+H2O,故A错误;B正确;醋酸是弱酸,应该是分子形式,故C错误;等物质的量的NaHCO3和Ca(OH)2溶液混合,HCO3-少,HCO3-前系数应该为1,正确的离子方程式是Ca2++HCO3-+OH-=CaCO3↓+H2O,故D错误;故选B。
考点:考查离子方程式正误判断。

练习册系列答案
相关题目
下列反应的离子方程式正确的是
A.工业上用电解法制备烧碱:2Cl一+H2O 2OH一+H2↑+Cl2↑ 2OH一+H2↑+Cl2↑ |
| B.用食醋除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2 O+ CO2↑ |
C.NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH- H2O+NH3↑ H2O+NH3↑ |
| D.铜溶于硫酸酸化的过氧化氢溶液:Cu+2H++H2O2=Cu2++2H2 O |
下列离子方程式书写不正确的是
A.向溴化亚铁溶液中通入过量氯气: |
B.氯化亚铁溶液与过氧化钠2:1反应: |
C.向氧化铁中加入氢碘酸发生反应: |
D.过量铁粉与稀HNO3反应: |
下列各组离子在溶液中能够大量共存,当溶液中c(H+)=10-1 mol·L-1时有气体产生;而当溶液中c(H+)=10-13 mol·L-1时又能生成沉淀。则该组离子可能是( )
| A.Na+、Ba2+、NO3-、CO32- |
| B.Ba2+、K+、Cl-、NO3- |
| C.Mg2+、NH4+、SO42-、Cl- |
| D.Fe2+、Na+、SO42-、NO3- |
下列各组离子能大量共存的是( )
| A.pH<7的溶液中:Na+、S2-、K+、MnO4— |
| B.pH=7的溶液中:Al3+、Cl-、SO42—、AlO2— |
| C.pH>7的溶液中:Na+、CO32—、SO32—、K+ |
| D.pH=0的溶液中:Na+、Al3+、Fe2+、ClO- |
常温下,下列各组离子在有关限定条件下溶液中一定能大量共存的是( )
| A.由水电离产生的c(H+)=10-12 mol/L的溶液中:K+、Na+、ClO-、I- |
B.c(H+)=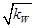 mol/L的溶液中:K+、Fe3+、Cl-、CO32— mol/L的溶液中:K+、Fe3+、Cl-、CO32— |
C.常温下,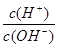 =1×10-12的溶液:K+、AlO2—、CO32—、Na+ =1×10-12的溶液:K+、AlO2—、CO32—、Na+ |
| D.pH=13的溶液中:AlO2—、Cl-、HCO3—、SO42— |
下列离子方程式或化学方程式与所述事实相符且正确的是( )
| A.H218O中投入Na2O2固体:2H218O+2O22—=4OH-+18O2↑ |
| B.向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:H++OH-=H2O |
| C.以金属银为阳极电解饱和硫酸铜溶液:Cu2++2H2O=2Cu+O2↑+4H+ |
| D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42—完全沉淀:Al3++2SO42—+2Ba2++4OH-=AlO2—+2BaSO4↓+2H2O |
下列有关的离子方程式中正确的是( )
| A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2—+4NH4++2H2O |
B.铜片接电源正极,碳棒接电源负极,电解硫酸溶液:Cu+2H+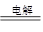 Cu2++H2↑ Cu2++H2↑ |
C.磷酸一氢钠溶液水解:HPO42—+H2O PO43—+H3O+ PO43—+H3O+ |
| D.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
下表对某些反应方程式的评价合理的是( )
| 编号 | 实验 | 离子方程式或电极反应式 | 评价 |
| A | 次氯酸钙溶液中通入足量SO2 | Ca2++ClO-+SO2+H2O CaSO4↓+Cl-+2H+ CaSO4↓+Cl-+2H+ | 正确 |
| B | Ba(OH)2溶液中加入过量Al2(SO4)3溶液 | 3Ba2++6OH-+2Al3++3S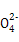  3BaSO4↓+2Al(OH)3↓ 3BaSO4↓+2Al(OH)3↓ | 正确 |
| C | 醋酸铵溶于水 | CH3COO-+N  CH3COOH+NH3·H2O CH3COOH+NH3·H2O | 错误,阴阳离子水解相互促进,应该用“ ”号 ”号 |
| D | 用惰性电极电解氯化铜和氯化钠的混合溶液一段时间 | 阴极:Cu2++2e- Cu Cu阳极:4OH--4e-  2H2O+O2↑ 2H2O+O2↑ | 错误,只因为两极得失电子没配平 |