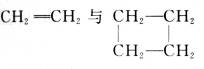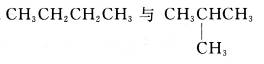题目内容
一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6 g,当其缓缓通过无水CaCl2时,CaCl2的质量增加22.5 g。原混合气体中CO2的质量为( )
| A.13.2 g | B.26.4 g | C.19.7 g | D.24.4 g |
B
n(H2O)=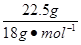 ="1.25" mol,所含氢原子为2.5 mol。根据氢原子守恒,则n(CH4)=
="1.25" mol,所含氢原子为2.5 mol。根据氢原子守恒,则n(CH4)= 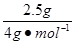 ="0.625" mol。设生成的CO、CO2的物质的量分别为x、y,则有
="0.625" mol。设生成的CO、CO2的物质的量分别为x、y,则有
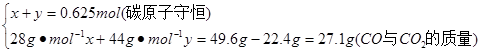
解得x="0.025" mol,y="0.6" mol,则m(CO2)="0.6" mol×44 g·mol-1="26.4" g。
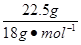 ="1.25" mol,所含氢原子为2.5 mol。根据氢原子守恒,则n(CH4)=
="1.25" mol,所含氢原子为2.5 mol。根据氢原子守恒,则n(CH4)= 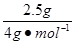 ="0.625" mol。设生成的CO、CO2的物质的量分别为x、y,则有
="0.625" mol。设生成的CO、CO2的物质的量分别为x、y,则有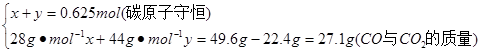
解得x="0.025" mol,y="0.6" mol,则m(CO2)="0.6" mol×44 g·mol-1="26.4" g。

练习册系列答案
相关题目