题目内容
如图所示甲、乙是电化学实验装置。
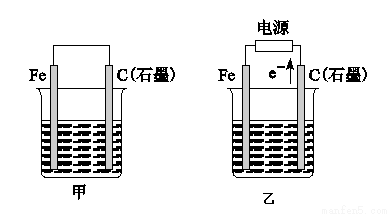
(1) 若甲、乙两烧杯中均盛有NaCl溶液。
① 甲中石墨棒上的电极反应式为______________________________;
② 乙中总反应的离子方程式为________________________________;
③ 将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为________________________
(2) 若甲、乙两烧杯中均盛有CuSO4溶液。
① 甲中铁棒上的电极反应式为___________________________;
② 如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的H变为1,若要使溶液恢复到电解前的状态,可向溶液中加入__________(填写物质的化学式)________g。
(1)用不到的仪器 (填字母)
A.烧杯 |
B.托盘天平 |
C.量筒 |
D.胶头滴管 |
E.玻璃棒
F.500mL容量瓶;
(2)实验开始前需要检验容量瓶 ;
(3)需要量取浓硫酸的体积为 ;
(4)将量取的浓硫酸沿烧杯壁慢慢注入盛有适量水的烧杯中,并不断搅拌,然后________________;
(5)将上述烧杯中的硫酸溶液转移至容量瓶时,某实验小组同学操作的示意图如下。请你指出图中错误。_______________________;
(6)某实验小组其它操作均正确,但未用蒸馏水洗涤烧杯,则其所配制溶液的浓度 ;定容时若仰视刻度线,则所配制溶液的浓度____________(填“偏大”、“偏小”或“无影响”);
(7)溶液转移及洗涤完成后,应向容量瓶中直接加水到离刻度线下__________时,改用胶头滴管加水,使溶液的凹液面正好跟刻度线水平相切。
下列实验方案中,能达到实验目的的是( )
选项 | 实验目的 | 实验方案 |
A | 证明氧化性:H2O2比Fe3+强 | 用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
B | 鉴别KBr溶液和KI溶液 | 分别加入新制氯水,再加入CCl4振荡、静置,观察 |
C | 配制100 mL 1.0 mol·L-1 CuSO4溶液 | 将25 g CuSO4·5H2O溶于100 mL蒸馏水中 |
D | 除去CuO中混有的Al2O3: | 加入过量盐酸溶液后,过滤 |
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
①可以判断该分解反应已经达到化学平衡的是___________。
A.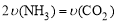
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:__________________________。
③氨基甲酸铵分解反应的焓变△H_________0,熵变△S________0(填>、<或=)。
(2)已知:NH2COONH4+2H 2O
2O NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始 浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。

计算25℃时,0~6min氨基甲酸铵水解反应的平均速率_______________________。


 c(Na+)>c(A-)>c(H+)>c(OH-)
c(Na+)>c(A-)>c(H+)>c(OH-)
 N2(g)+9O2(g)=2C3H5(ONO2)3(l) △H1
N2(g)+9O2(g)=2C3H5(ONO2)3(l) △H1
 2OH-+H2↑
2OH-+H2↑