题目内容
5. 为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究性学习:
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究性学习:【查阅资料】金属活泼性不同,其硝酸盐分解产物不同
(1)K→Na活泼金属的硝酸盐分解生成亚硝酸盐和氧气;
(2)Mg→Cu等较活泼金属的硝酸盐分解生成氧化物、NO2和O2;
(3)Hg以后不活泼金属的硝酸盐分解生成金属、NO2和O2.
2KNO3$\frac{\underline{\;\;△\;\;}}{\;}$2KNO2↑+O2↑
2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑
2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑
I:【实验一】探究Fe(NO3)2热分解固体产物中Fe元素的价态.该小组甲同学将其溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验.①向一份溶液中滴入少量KSCN溶液;②少量稀酸性KMnO4溶液中滴入另一份溶液.现象:①溶液变红色②KMnO4溶液颜色无明显变化
(1)则Fe(NO3)2分解的化学方程式是4Fe(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8NO2↑+O2↑
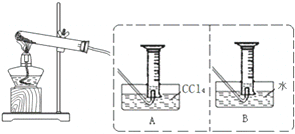
II:【实验二】探究Fe(NO3)2热分解气体产物的性质.小组乙、丙同学进行了如图所示的实验(收集时操作恰当,几乎没有空气)
实验步骤:①连接仪器;②检查装置气密性;③取一定质量Fe(NO3)2装于大试管,并重新连接好仪器;④加热;⑤…
(2)乙同学使用A装置收集气体,恰好收集到54mL红棕色气体,要从水槽中取出量筒,乙同学的正确操作方法是用玻璃片在水槽里盖好量筒口,用食指摁紧玻璃片,将量筒从水槽中取出,正放在试验台上
(3)丙同学取等质量Fe(NO3)2的在同样条件下热分解,用B装置收集气体产物,可收集到气体8mL.
III:【实验三】探究固体混合物的组成和特征
(4)小组丁同学取KNO3、Cu(NO3)2、Fe(NO3)2混合粉末充分加热后用排水法未收集到任何气体,则KNO3、Cu(NO3)2、Fe(NO3)2物质的量之比可能为A.
A.1:2:2 B.2:1:3 C.1:2:3 D.3:8:5
(5)取0.6mol由KNO3、Cu(NO3)2、Fe(NO3)3按等物质的量之比混合而成的粉末溶于100mL 3mol/L的稀硫酸中,再向溶液中加入足量的铜粉,则最多可溶解铜粉质量为20.8g.
分析 (1)向一份溶液中滴入少量KSCN溶液,溶液变红色,说明有铁离子产生成,根据电子得失守恒可知Fe(NO3)2热分解生成了氧化铁,二氧化氮和氧气,据此答题;
(2)由于NO2和的密度均大于空气,所以将量筒从水槽中取出,正放在试验台上;
(3)由4Fe(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8NO2↑+O2↑可知产生NO2和O2的体积比为8:1,而4NO2~O2可恰好进入溶液中,剩余的NO2溶于水产生NO,因此收集到的气体为NO;
(4)根据三个反应2KNO3$\frac{\underline{\;\;△\;\;}}{\;}$2KNO2↑+O2↑;2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑; 2Fe(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+8NO2↑+O2↑,混合粉末充分加热后用排水法未收集到任何气体,说明三个反应中生成的气体物质的量之比n(NO2):n(O2)=4:1,通过选项答案验证;
(5)0.6mol由KNO3、Cu(NO3)2、Fe(NO3)3按等质的量之比混合,即各为0.2mol,所以溶液中硝酸根离子的物质的量为1.2mol,溶液中加入铜粉后发生的反应有3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O、Cu+2Fe3+=Cu2++2Fe2+,根据方程式计算.
解答 解:(1)向一份溶液中滴入少量KSCN溶液,溶液变红色,说明有铁离子产生成,根据电子得失守恒可知Fe(NO3)2热分解生成了氧化铁,二氧化氮和氧气,方程式为:4Fe(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8NO2↑+O2↑,
故答案为:4Fe(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8NO2↑+O2↑;
(2)将收集气体的量筒从水槽中取出的方法是用玻璃片在水槽里盖好量筒口,用食指摁紧玻璃片,由于NO2和的密度均大于空气,所以将量筒从水槽中取出,正放在试验台上,
故答案为:用玻璃片在水槽里盖好量筒口,用食指摁紧玻璃片,将量筒从水槽中取出,正放在试验台上;
(3)若用排水法收集时,4NO2~O2可恰好进入溶液中,由4Fe(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$ 2Fe2O3+8NO2↑+O2↑可知产生NO2和O2的体积比为8:1,则54ml气体中有24ml NO2和6ml O2恰好进入溶液,另外24ml NO2溶于水产生8ml NO,则收集到的气体为8ml 气体,
故答案为:8;
(4)根据三个反应2KNO3$\frac{\underline{\;\;△\;\;}}{\;}$2KNO2↑+O2↑;2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑; 2Fe(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+8NO2↑+O2↑,混合粉末充分加热后用排水法未收集到任何气体,说明三个反应中生成的气体物质的量之比n(NO2):n(O2)=4:1,Cu(NO3)2受热分解的气体产物恰好符合物质的量之比n(NO2):n(O2)=4:1,所以其量为任意值,而KNO3和Fe(NO3)2按物质的量比为1:2混合受热分解的气体恰好符合n(NO2):n(O2)=4:1进入溶液,
故答案为:A;
(5)0.6mol由KNO3、Cu(NO3)2、Fe(NO3)3按等质的量之比混合,即各为0.2mol,所以溶液中硝酸根离子的物质的量为1.2mol,100mL 3mol/L的稀硫酸中,氢离子的物质的量为0.6mol,根据反应3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O可知,溶液中硝酸根离子过量,所以此反应中溶解的铜的质量为$\frac{0.6}{8}$g=14.4g,Fe(NO3)3的质的量为0.2mol,根据反应Cu+2Fe3+=Cu2++2Fe2+,此反应中溶解的铜的质量为$\frac{1}{2}$×0.2×64g=6.4g,所以总共溶解的铜的质量为6.4g+14.4g=20.8g,
故答案为:20.8g.
点评 本题考查了铁及其重要化合物的性质实验方案设计,侧重于离子检验、设计实验方案及操作、混合物的计算,综合性较强,难度较大,计算Cu的质量时注意硝酸根离子是过量的.

| A. | 加水稀释到1000ml | B. | 加入10ml0.1mol/L的氨水 | ||
| C. | 加入100ml0.005mol/L的Ba(OH)2溶液 | D. | 加入100ml0.05mol/L的NaOH溶液 |
| A. | 若c1=2c2,则w1<2w2,V<50mL | B. | 若c1=2c2,则w1<2w2,V=50mL | ||
| C. | 若w1=2w2,则c1<2c2,V>50mL | D. | 若w1=2w2,则c1>2c2,V<50mL |
| A. | 0.2 mol/L CH3COONa溶液和0.1 mol/L HCl溶液等体积混合后:c(CH3COO-)>c(Na+)>c(Cl-)>c(H+)>c(OH-) | |
| B. | pH=3的盐酸和NaNO3的混合溶液中:c(Na+)=c(Cl-) | |
| C. | 0.1 mol/L NaHCO3溶液中:c(Na+)+c(H+)═c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 物质的量浓度相等的HCN(弱酸)和NaCN溶液等体积混合后有:c(HCN)+2c(H+)═2c(OH-)+c(CN-) |

 $→_{Fe}^{Br_{2}}$A$→_{K_{2}CO_{3}丙酮}^{B(CH_{2}=CHCH_{2}Br)}$
$→_{Fe}^{Br_{2}}$A$→_{K_{2}CO_{3}丙酮}^{B(CH_{2}=CHCH_{2}Br)}$ $→_{THF}^{Mg}$ $\stackrel{B}{→}$C$→_{2H_{3}O+}^{1Li,THF,室温}$D
$→_{THF}^{Mg}$ $\stackrel{B}{→}$C$→_{2H_{3}O+}^{1Li,THF,室温}$D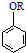 $→_{H_{3}O+}^{Li,THF,室温}$
$→_{H_{3}O+}^{Li,THF,室温}$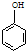

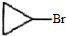 是B的一种同分异构体,核磁共振氢谱证明它有2种不同的化学环境的氢.
是B的一种同分异构体,核磁共振氢谱证明它有2种不同的化学环境的氢.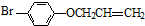 的反应类型取代反应.
的反应类型取代反应.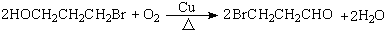 .
.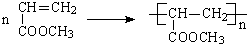 .
. .
.