题目内容
分子式为CnH2nO2的一元羧酸0.568克,恰好中和0.1摩/升的苛性钠溶液20毫升,则n值是( )
分析:一元羧酸和氢氧化钠中和的物质的量之比是1:1,根据碱的量可以确定羧酸的量,进而获得羧酸的相对分子质量,求的结果即可.
解答:解:从分子式为CnH2nO2可知该羧酸分子只含1个-COOH(羧基),1mol该羧酸可与1molNaOH反应,NaOH的物质的量为:0.1mol/L×0.02L=0.002mol,则与之反应的羧酸物质的量也为0.002mol,
该羧酸的摩尔质量为:
=284g/mol,即12n+2n+32=284,n=18,所以该羧酸为C18H36O2.
故选D.
该羧酸的摩尔质量为:
| 0.568g |
| 0.002g/mol |
故选D.
点评:本题涉及有机物分子式的确定知识,注意酸碱中和的实质以及质量和物质的量之间的关系是解题的关键,难度不大.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
 的数目为NA
的数目为NA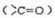
 的数目为NA
的数目为NA )的数目为NA
)的数目为NA