题目内容
【题目】某同学配制500 mL 0.5 mol/L NaOH溶液。
(1)该同学在实验过程中,用到的玻璃仪器有:量筒、玻璃棒、胶头滴管、烧杯___________。
(2)其操作步骤如乙图所示,则甲图操作应在乙图中的 ____ (填选项字母)之间。
A.①与② B.②与③ C.④与⑤ D.⑤与⑥


(3)该同学应称取NaOH固体 ___ g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小_____(填小写字母),
附表:砝码规格

a | b | c | d | e | |
砝码大小/g | 100 | 50 | 20 | 10 | 5 |
并在下图中选出能正确表示游码位置的选项 ____ (填大写字母)。


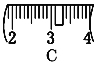
该同学实际配制NaOH溶液的浓度为0.48 mol·L-1,原因可能是 ____ (填序号)。
A.称量NaOH固体时,采用了“左码右物” B.容量瓶中原来存有少量水
C.溶解固体的烧杯移液后未洗涤 D.用胶头滴管加水定容时仰视刻度
【答案】 500mL容量瓶 C 10.0 g cd C ACD
【解析】(1)配制时应该选用500mL的容量瓶,配制步骤有:计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,(可能会用到量筒量取蒸馏水),冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的玻璃仪器为:量筒、玻璃棒、胶头滴管、烧杯、500mL容量瓶,所以还缺填500mL容量瓶;(2)甲图操作为直接向容量瓶中加水定容,应该放在使用胶头滴管定容之前,即④与⑤之间,故答案为:C;(3)配制500mL 0.5mol/L NaOH溶液,需要氢氧化钠的质量为:40g/mol×0.5mol/L×0.5L=10.0g;用质量为23.1g的烧杯放在托盘天平上称取所需NaOH固体时,烧杯和氢氧化钠的总质量为:23.1g+10.0g=33.1g,需要选用的砝码为20g+10g,即cd正确;还需要游码的质量为:33.1g-30g=3.1g,图示中C的游码读数为3.1g,所以答案选C;(4)A.称量NaOH固体时,采用了“左码右物”,导致称量的氢氧化钠的质量偏小,配制的溶液中氢氧化钠的物质的量偏小,溶液浓度偏低,选项A正确;B.容量瓶中原来存有少量水,对溶质的物质的量及溶液的体积都没有影响,所以不影响配制结果,选项B错误;C.溶解固体的烧杯移液后未洗涤,导致配制的溶液中溶质氢氧化钠的物质的量偏小,配制的溶液浓度偏低,选项C正确;D.用胶头滴管加水定容时仰视刻度,导致配制时加入的蒸馏水体积偏大,配制的溶液浓度偏低,选项D正确;答案选ACD。

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】前四周期的A、B、C、D四种元素在周期表中均与元素X紧密相邻。已知元素X最高价氧化物的化学式为X2O5,B、D同主族且B元素的原子半径是同族元素中最小的,C的最高价氧化物对应的水化物是强酸。
(1)D元素基态原子的外围电子排布式为____________________。
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为________________(用相应的元素符号作答)。
(3)B、X、D氢化物的沸点由高到低的顺序为_______________(用相应的化学式作答)。
(4)C元素的原子可形成多种离子,试推测下列微粒的立体构型(C为字母,不是碳元素):
微粒 | CO32- | CO42- |
立体构型名称 | _______________ | _______________ |
(5)元素B的一种氢化物B2H4具有重要的用途。有关B2H4的说法正确的是_______。
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
(6)E元素和D元素在同一周期,属于VIII族,价层有三个单电子,E(OH)2为两性氢氧化物,在浓的强碱溶液中可形成E(OH)42-,写出E(OH)2酸式电离的电离方程式___________________。
(7)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如图所示)中F原子的配位数之比为___________,δ、γ、α三种晶胞的边长之比为_____________。


