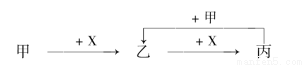
题目内容
现有25 mL 2 mol·L-1 Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中;②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况是( )。
A.均为0.84 L B.均为0.56 L
C.①>② D.②>①
C
【解析】①将Na2CO3溶液逐滴加入到盐酸中,开始时,HCl过量,有关反应为:
Na2CO3+ 2HCl=2NaCl+CO2↑+H2O
1 mol 2 mol 22.4 L
0.05 mol 0.075 mol V1
生成CO2的体积用HCl的量计算:
V1=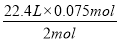 =0.84 L
=0.84 L
②将盐酸逐滴加入到Na2CO3溶液中,开始时,Na2CO3过量,反应分两步进行:
Na2CO3+ HCl = NaHCO3+NaCl
1 mol 1 mol 1 mol
0.05 mol 0.05 mol 0.05 mol
NaHCO3+ HCl=NaCl+H2O+CO2↑
1 mol 1 mol 22.4 L
0.05 mol (0.075-0.05)mol V2
生成的CO2用剩余HCl的量计算:
V2=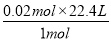 =0.56 L,所以V1>V2。
=0.56 L,所以V1>V2。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案某无色稀溶液X中,可能含有下表所列离子中的某几种。
阴离子 | CO32-、SiO32-、AlO2-、Cl- |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系图所示。
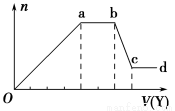
(1)若Y是盐酸,则Oa段转化为沉淀的离子(指来源于X溶液的,下同)是 ,
ab段发生反应的离子是 ,bc段发生反应的离子方程式为 。
(2)若Y是NaOH溶液,则X中一定含有的离子是 ,ab段反应的离子方程式为 。