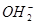题目内容
按图的装置连接好仪器,先在烧杯中加入20mL左右的Ba(OH)2溶液,接通电源后,逐渐滴加稀硫酸至过量。
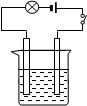
(1)当逐渐滴加稀硫酸时,烧杯中观察到的现象是: 。
(2)灯泡的现象是: ;原因是: 。
(3)发生反应的离子方程式为:

(1)当逐渐滴加稀硫酸时,烧杯中观察到的现象是: 。
(2)灯泡的现象是: ;原因是: 。
(3)发生反应的离子方程式为:
(1)生成白色沉淀
(2)先变暗后变亮 Ba(OH)2和H2SO4先发生反应使离子浓度减小,然后H2SO4过量离子浓度增大
(3)Ba2++SO42-+ 2OH-+2H+= BaSO4↓+2H2O
(2)先变暗后变亮 Ba(OH)2和H2SO4先发生反应使离子浓度减小,然后H2SO4过量离子浓度增大
(3)Ba2++SO42-+ 2OH-+2H+= BaSO4↓+2H2O
试题分析:向Ba(OH)2溶液中,逐滴加入稀硫酸,先生成BaSO4沉淀,溶液的导电性减弱,所以灯泡先变暗;稀硫酸过量时,溶液中H+和SO42-浓度增大,灯泡又变亮。

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目