题目内容
由一氧化碳、甲烷和乙烷组成的混合气体6.72L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸.再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重22g,则原混合气体中乙烷的物质的量为
- A.0.1mol
- B.等于0.2mol
- C.大于或等于0.2mo1,小于0.3mol
- D.不能确定
B
分析:一氧化碳、甲烷和乙烷组成的混合气体6.72L(标准状况),混合气体的物质的量为0.3mol,混合气体在足量氧气中充分燃烧生成二氧化碳和水.NaOH溶液吸收二氧化碳,所以NaOH溶液增重22克为二氧化碳质量,结合二氧化碳质量根据碳原子守恒计算甲碳原子平均数,根据平均碳原子,利用十字交叉法计算乙烷的物质的量.
解答:一氧化碳、甲烷和乙烷组成的混合气体6.72L(标准状况),混合气体的物质的量为 =0.3mol.
=0.3mol.
NaOH溶液吸收二氧化碳,故NaOH溶液增重22克为二氧化碳质量,所以二氧化碳的物质的量为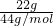 =0.5mol.
=0.5mol.
所以平均组成中平均碳原子数为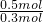 =
=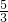 ,
,
一氧化碳、甲烷分子中都含有一个碳原子,可以看做1个组分,

所以一氧化碳、甲烷的总物质的量与乙烷的物质的量之比为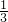 :
: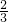 =1:2.
=1:2.
所以混合物中乙烷的物质的量为0.3mol×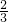 =0.2mol.
=0.2mol.
故选:B.
点评:考查烃混合物分子式确定,难度较大,注意利用平均分子组成判断烃的组成,常用方法有1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法.
分析:一氧化碳、甲烷和乙烷组成的混合气体6.72L(标准状况),混合气体的物质的量为0.3mol,混合气体在足量氧气中充分燃烧生成二氧化碳和水.NaOH溶液吸收二氧化碳,所以NaOH溶液增重22克为二氧化碳质量,结合二氧化碳质量根据碳原子守恒计算甲碳原子平均数,根据平均碳原子,利用十字交叉法计算乙烷的物质的量.
解答:一氧化碳、甲烷和乙烷组成的混合气体6.72L(标准状况),混合气体的物质的量为
 =0.3mol.
=0.3mol.NaOH溶液吸收二氧化碳,故NaOH溶液增重22克为二氧化碳质量,所以二氧化碳的物质的量为
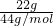 =0.5mol.
=0.5mol.所以平均组成中平均碳原子数为
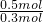 =
=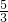 ,
,一氧化碳、甲烷分子中都含有一个碳原子,可以看做1个组分,

所以一氧化碳、甲烷的总物质的量与乙烷的物质的量之比为
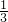 :
: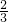 =1:2.
=1:2.所以混合物中乙烷的物质的量为0.3mol×
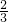 =0.2mol.
=0.2mol.故选:B.
点评:考查烃混合物分子式确定,难度较大,注意利用平均分子组成判断烃的组成,常用方法有1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法.

练习册系列答案
相关题目
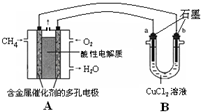
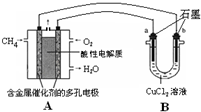 (2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.
(2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.