题目内容
已知元素X的基态原子最外层电子排布为nsn-1npn+2,则它最高价氧化物对应的水化物的酸根离子是( )A.RO
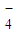
B.RO43-
C.RO

D.RO32-
【答案】分析:nsn-1应排满,为2个电子,故n=3,元素X的基态原子最外层电子排布为3s2np5.
解答:解:nsn-1应排满,为2个电子,故n=3,元素X的基态原子最外层电子排布为3s2np5,为Cl元素,最高化合价为+7价,故选A.
点评:本题考查原子结构与元素的性质,难度不大,注意根据构造原理,先排能量低的再排能量高的.
解答:解:nsn-1应排满,为2个电子,故n=3,元素X的基态原子最外层电子排布为3s2np5,为Cl元素,最高化合价为+7价,故选A.
点评:本题考查原子结构与元素的性质,难度不大,注意根据构造原理,先排能量低的再排能量高的.

练习册系列答案
相关题目
已知元素X的基态原子最外层电子排布为nsn-1npn+2,则X元素的原子序数为
| A.9 | B.10 | C.17 | D.18 |