题目内容
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。K2FeO4为紫色固体,微溶于KOH溶液。K2FeO4具有强氧化性,在酸性或中性溶液中迅速产生O2,在碱性溶液中较稳定。某学习小组设计了下面的实验制备K2FeO2并探究其性质。
Ⅰ.K2FeO4的制备
该小组用如图所示装置制备K2FeO4(夹持装置略)。
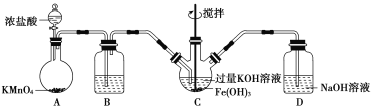
(1)以上装置图中有一处明显的错误请你帮助指出来:___________。B中应盛装的试剂是___________。
(2)写出A中发生反应的离子方程式__________________________________。
(3)C中发生的反应有Cl2+2OH-===Cl-+ClO-+H2O,还有生成K2FeO4的反应。写出得到紫色固体K2FeO4的化学方程式为____________。
Ⅱ.性质探究
用KOH溶液充分洗涤C中所得固体得到固体物质K2FeO4。
(4)絮凝实验:甲同学取少量K2FeO4加入浑浊的泥浆水中,发现产生气体,搅拌,浑浊的泥浆水很快澄清。请结合方程式,说明K2FeO4的净水原理:_________________。
(5)乙同学取少量K2FeO4,向其中滴入稀盐酸发现产生黄绿色气体。产生黄绿色气体的原因可能是___。
(6)丙同学取少量K2FeO4,向其中滴入MnSO4和适量H2SO4的混合溶液,振荡后溶液呈紫色,丙同学认为氧化性FeO42->MnO4-。请你设计一个实验,验证丙同学的结论是否正确:_____________
【答案】D中没有出气导管 饱和氯化钠溶液 2MnO4-+16H++10Cl-===2Mn2++5Cl2↑+8H2O 3Cl2+2Fe(OH)3+10KOH===2K2FeO4+6KCl+8H2O K2FeO4与水发生反应 4FeO42-+10H2O===4Fe(OH)3(胶体)+3O2↑+8OH-,产生的 Fe(OH)3胶体可以吸附水中悬浮的杂质使水澄清 K2FeO4有强氧化性,将Cl-氧化为氯气 取少量紫色溶液滴加过量稀H2SO4,若溶液紫色不褪去,则丙同学的结论正确;若溶液紫色快速褪去,则丙同学的结论不正确
【解析】
Ⅰ.由图可知,A中浓盐酸与高锰酸钾发生2MnO4-+10Cl-+16H+═5Cl2↑+2Mn2++8H2O,可制备氯气,B中饱和食盐水可除去挥发的HCl,C中碱性条件下氯气与氢氧化铁反应生成K2FeO4,D中NaOH可吸收过量氯气;
Ⅱ.(4)K2FeO4具有强氧化性,且还原产物水解生成胶体;
(5)K2FeO4,向其中滴入稀盐酸发现产生黄绿色气体,气体为氯气,发生氧化还原反应;
(6)取少量K2FeO4,向其中滴入MnSO4和适量H2SO4的混合溶液,振荡后溶液呈紫色,可知生成高锰酸根离子,继续加硫酸可说明。
(1)题图装置图中D中只有进气导管,没有出气导管;高锰酸钾与浓盐酸反应产生的氯气中混有较多的氯化氢气体,对C中的反应有不良影响,因此,B中应盛装的试剂是饱和氯化钠溶液。
(2)高锰酸钾与浓盐酸反应产生氯气、KCl、MnCl2和水,根据电子守恒和原子守恒配平,A中的反应化学方程式为2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,离子方程式为2MnO![]() +16H++10Cl-===2Mn2++5Cl2↑+8H2O。
+16H++10Cl-===2Mn2++5Cl2↑+8H2O。
(3)C中Fe(OH)3、KOH和氯气反应生成K2FeO4,铁元素从+3价升高为+6价,被氧化,因此氯气作氧化剂,其还原产物是氯化钾,化学方程式为3Cl2+2Fe(OH)3+10KOH===2K2FeO4+6KCl+8H2O。
(4)甲同学取少量K2FeO4加入浑浊的泥浆水中,发现产生气体,搅拌,浑浊的泥浆水很快澄清,是因为K2FeO4与水发生反应 4FeO42-+10H2O===4Fe(OH)3(胶体)+3O2↑+8OH-,产生的Fe(OH)3胶体可以吸附水中悬浮的杂质使水澄清。
(5)乙同学取少量K2FeO4,向其中滴入稀盐酸发现产生黄绿色气体。产生黄绿色气体的原因可能是K2FeO4有强氧化性,将Cl-氧化为氯气。
(6)丙同学取少量K2FeO4,向其中滴入MnSO4和适量H2SO4的混合溶液,振荡后溶液呈紫色,说明生成了MnO4-,据题目所提供的资料可知K2FeO4具有强氧化性,在酸性或中性溶液中迅速产生O2,在碱性溶液中较稳定。为了验证丙同学的想法是否正确,可以取少量紫色溶液滴加过量稀H2SO4,若溶液紫色不褪去,则丙同学的结论正确;若溶液紫色快速褪去,则丙同学的结论不正确。

 阅读快车系列答案
阅读快车系列答案【题目】已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O.如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在 KClO3 晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是 ( )
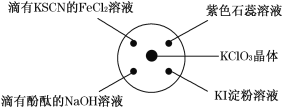
选项 | 实验现象 | 结论 |
A | 滴有 KSCN 的 FeCl2 溶液变红色 | Cl2 具有还原性 |
B | 滴有酚酞的 NaOH 溶液褪色 | Cl2 具有酸性 |
C | 淀粉 KI 溶液中变蓝色 | Cl2 具有氧化性 |
D | 石蕊溶液先变为红色后褪色 | Cl2 具有漂白性 |
A. A B. B C. C D. D