题目内容
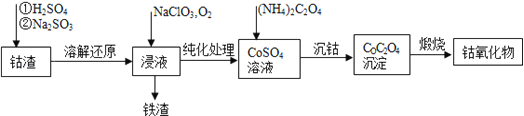
【题目】利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)制备铁红,大致生产过程如下:

请回答:
⑴检验滤液A 中含有Fe2+的方法是 。
⑵滤液A→B发生反应的离子方程式为 。
⑶在空气中煅烧FeCO3的方程式为 。
【答案】
⑴取少量滤液A于试管中,向试管中滴加酸性高锰酸钾溶液,若溶液褪色,则说明存在Fe2+。
⑵ 2Fe3+ + Fe = 3Fe2+
(3)4FeCO3 +O2![]() 2Fe2O3 +4CO2
2Fe2O3 +4CO2
【解析】
试题分析:⑴检验溶液是否含有Fe2+的方法是取少量滤液A于试管中,向试管中滴加酸性高锰酸钾溶液,若溶液褪色,则说明存在Fe2+,故答案为:取少量滤液A于试管中,向试管中滴加酸性高锰酸钾溶液,若溶液褪色,则说明存在Fe2+;
⑵酸浸后滤液A主要含有硫酸铁,硫酸亚铁,加入试剂a后得到硫酸亚铁,因此试剂a为铁,滤液A→B发生反应的离子方程式为2Fe3+ + Fe = 3Fe2+,故答案为:2Fe3+ + Fe = 3Fe2+;
⑶空气中煅烧FeCO3生成铁红,反应的方程式为4FeCO3 +O2![]() 2Fe2O3 +4CO2,故答案为:4FeCO3 +O2
2Fe2O3 +4CO2,故答案为:4FeCO3 +O2![]() 2Fe2O3 +4CO2。
2Fe2O3 +4CO2。

练习册系列答案
相关题目