题目内容
(8分)有一包白色固体,可能是、K2CO3、K2SO4、CuSO4和中的一种或几种。将此白色固体溶解于水时,有生成,过滤后,滤液为无色。
①将部分沉淀移入试管中,加入稀硝酸,沉淀溶解完全,且有气体生成。
②在滤液中滴入几滴AgNO3溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
通过上述实验现象分析:该白色固体中一定含有的物质为 ,不可能含有的物质为 ,不能确定的物质是 ,为了确定该物质是否存在,可以通过
实验确定。
①将部分沉淀移入试管中,加入稀硝酸,沉淀溶解完全,且有气体生成。
②在滤液中滴入几滴AgNO3溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
通过上述实验现象分析:该白色固体中一定含有的物质为 ,不可能含有的物质为 ,不能确定的物质是 ,为了确定该物质是否存在,可以通过
实验确定。
K2CO3、BaCl2; K2SO4、CuSO4;NaCl;焰色反应
滤液为无色说明一定不含CuSO4,白色沉淀加入稀硝酸,沉淀溶解完全说明一定含有BaCl2,K2CO3,一定不含K2SO4(生成硫酸钡沉淀,不溶于硝酸)。不能确定的是NaCl,检验其必须用焰色反应。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
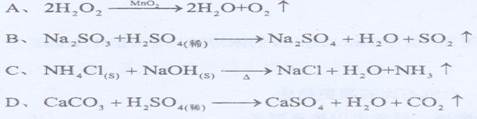
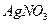 溶液检验两瓶均为红棕色的气体:
溶液检验两瓶均为红棕色的气体: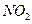 和
和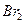 蒸汽
蒸汽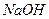 溶液清洗
溶液清洗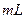 98%的浓
98%的浓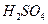 ,向其中加水稀释至8Ml
,向其中加水稀释至8Ml